
【题目】A~G都是有机化合物,它们的转化关系如下:
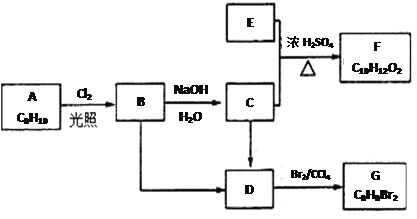
已知:E是生活中常见的有机物,是一种弱电解质。A为一取代芳烃,B中含有一个甲基。
请回答下列问题:
(1)D的名称是___________;E所含的官能团是_______________________(填名称)。
(2)F的结构简式________________________。
(3)由B生成D的化学方程式为________________________;反应类型是_________。
(4)检验B中官能团的方法是____________________________________________。
(5)在G的同分异构体中,苯环上一硝化的产物只有一种的共有_______种,其中核磁共振氢谱有两组峰,且峰面积比为l:1的是____________________(填结构简式)。
A的最简单的同系物H与液溴反应生成M,M在一定的温度、压强下与氢氧化钠水溶液反应生成N,向N的水溶液中通入CO2生成有机物P。
(6)由M生成N的化学方程式为_____________________________________________。
(7)由N生成P的离子方程式为______________________________________________。
(8)定量测定P的化学原理是(用化学方程式表示)____________________________。
【答案】 乙烯 羧基 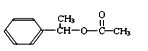
 消去反应 向试管中加入适量B,加入足量氢氧化钠溶液,加热,冷却后加稀硝酸酸化,滴加几滴硝酸银溶液,产生白色沉淀,证明B中有氯原子 7种
消去反应 向试管中加入适量B,加入足量氢氧化钠溶液,加热,冷却后加稀硝酸酸化,滴加几滴硝酸银溶液,产生白色沉淀,证明B中有氯原子 7种 ![]()
![]()
【解析】E是生活中常见的有机物,是一种弱电解质,则根据A与F的分子式可判断E可能是醋酸。A为一取代芳烃,与氯气在光照条件下发生苯环取代基上氢原子的取代反应生成B,B中含有一个甲基,B水解生成C。根据D与溴的四氯化碳溶液生成G的分子式可知该反应是加成反应,则D应该是苯乙烯,所以A是乙苯,B的结构简式为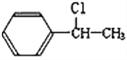 ,C的结构简式为
,C的结构简式为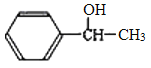 ,G的结构简式为
,G的结构简式为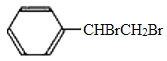 。C与乙酸发生酯化反应生成F,F的结构简式为
。C与乙酸发生酯化反应生成F,F的结构简式为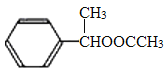 。
。
(1)根据以上分析可知D的名称是苯乙烯;乙酸所含的官能团是羧基。(2)F的结构简式为 。(3)由B生成D是卤代烃的消去反应,反应的化学方程式为
。(3)由B生成D是卤代烃的消去反应,反应的化学方程式为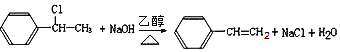 。(4)B中含有氯原子,则检验B中官能团的方法是向试管中加入适量B,加入足量氢氧化钠溶液,加热,冷却后加稀硝酸酸化,滴加几滴硝酸银溶液,产生白色沉淀,证明B中有氯原子。(5)在G的同分异构体中,苯环上一硝化的产物只有一种,说明结构对称。苯环可以是两个-CH2Br或2个甲基和2个溴原子,前者只能是处于对位。后者如果两个甲基相邻,有两种,两个甲基相间只有一种,如果两个甲基相对,则有3种,共有7种,其中核磁共振氢谱有两组峰,且峰面积比为l:1的是
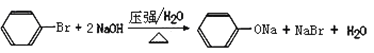
。(4)B中含有氯原子,则检验B中官能团的方法是向试管中加入适量B,加入足量氢氧化钠溶液,加热,冷却后加稀硝酸酸化,滴加几滴硝酸银溶液,产生白色沉淀,证明B中有氯原子。(5)在G的同分异构体中,苯环上一硝化的产物只有一种,说明结构对称。苯环可以是两个-CH2Br或2个甲基和2个溴原子,前者只能是处于对位。后者如果两个甲基相邻,有两种,两个甲基相间只有一种,如果两个甲基相对,则有3种,共有7种,其中核磁共振氢谱有两组峰,且峰面积比为l:1的是![]() 。(6)A的最简单的同系物H是苯,与液溴反应生成M是溴苯,溴苯在一定的温度、压强下与氢氧化钠水溶液反应生成N是苯酚钠,向苯酚钠的水溶液中通入CO2生成有机物P是苯酚,则由M生成N的化学方程式为
。(6)A的最简单的同系物H是苯,与液溴反应生成M是溴苯,溴苯在一定的温度、压强下与氢氧化钠水溶液反应生成N是苯酚钠,向苯酚钠的水溶液中通入CO2生成有机物P是苯酚,则由M生成N的化学方程式为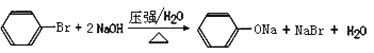 。(7)根据以上分析可知由N生成P的离子方程式为
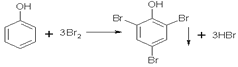
。(7)根据以上分析可知由N生成P的离子方程式为![]() 。(8)定量测定苯酚时可以用苯酚与浓溴水反应,化学方程式为
。(8)定量测定苯酚时可以用苯酚与浓溴水反应,化学方程式为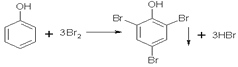 。
。


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说有关说法正确的是
A. 在常温常压下,11.2L N2含有的分子数小于0.5NA
B. 标准状况下,2.24L SO3含有的原子数为0.4NA
C. 将1L 2mol/L的FeCl3溶液,其中含有Cl-为2NA
D. 46g NO2和N2O4混合气体所含氧原子数目有可能为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
A.酸性氧化物:SO2、SO3、CO2、CO
B.碱:烧碱、纯碱、苛性钾、氢氧化钡
C.混合物:铝热剂、漂白粉、水煤气、氢氧化铁胶体
D.电解质:稀硫酸、氢氧化钠、氯化钠、MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生小红利用右下图装置合成乙酸乙酯的步骤如下:在圆底烧瓶A 内加入乙醇,浓硫酸和乙酸,瓶口竖直安装仪器B,加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:

(1)仪器B的名称为_____,冷凝水的流入方向是_______________(填“a”或“b”)。
(2)在烧瓶中放入碎瓷片,其作用是___________________;如果加热一段时间后发现忘记添加碎瓷片,应该采取的正确操作是___________(填字母)。
A.冷却后补加 B.立即补加 C.不需补加 D.重新配料后加入
(3)反应中加入过量乙醇,其目的是___________________。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是______________;浓硫酸用量又不能过多,原因是________________________。
(4)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是__________________________________。
(5)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯。他们分别将粗产品与一定量NaOH溶液混合后,蒸馏收集76℃~78℃的产品(已知:乙醇的沸点78℃,乙酸的沸点117.9℃,乙酸乙酯的沸点77℃)。实验结果:甲得到溶于水的液体X;乙得到难溶于水。但显酸性的液体Y;则:①X主要含_________________________。②Y主要_________________________。__________________________。
(6)丙同学重新设计了提纯粗产品的方案,流程如下:

由此回答下列问题:
①试剂a是:_______________ ,其作用是溶解乙醇、反应消耗乙酸和____________________。
②分离方法[Ⅰ]是_____________,试剂b是___________,分离方法[Ⅱ]是_____________。
(7)用30g乙酸与46g乙醇反应,产率为67%,则制得的乙酸乙酯的质量为__________g(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中由于哑铃形的C22﹣存在,使晶胞沿一个方向拉长.下列关于CaC2晶体的说法中正确的是( )

A. 1 个 Ca2+周围距离最近且等距离的 C22﹣数目为 6
B. 该晶体中的阴离子与F2是等电子体
C. 6.4 g CaC2晶体中含阴离子0.1 mol
D. 与每个Ca2+距离相等且最近的Ca2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如右图所示。以下有关该物质的说法中正确的是( )
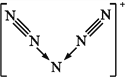
A. 每个N5+中含有35个质子和36个电子
B. 该离子中有非极性键和配位键
C. 该离子中含有2个π键
D. 与PCl4+互为等电子体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室需要480mL,0.5mol/L的稀硫酸,现欲用98%的浓硫酸(ρ=1.84g/cm3 )配制,配制步骤包括:①计算所用浓硫酸的体积②转移③定容、上下颠倒摇匀④量取一定体积的浓硫酸⑤洗涤并转移⑥稀释并冷却至室温⑦轻摇混匀。完成下列问题:
(1)正确的操作顺序为(填入序号)________。选用的主要仪器有:量筒、烧杯、玻璃棒、________、________。
(2)应量取浓硫酸的体积为________;量取浓硫酸所用的量筒的规格是________(从下列中选用,填字母 A.10 mL B.25 mL C.50 mL D.100 mL);第⑥步中稀释实验的操作方法是________。
(3)下列关于容量瓶的使用方法中,正确的是________。
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液要用玻璃棒引流
(4)下列情况中,所配制的稀硫酸浓度偏大的是________。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.用量筒量取浓硫酸时仰视刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 0.1mol/LNa2CO3溶液1L所含阴离子数目小于0.1NA
B. 常温常压下,3.2gCH4中含有的电子数为2NA
C. 1molCl2溶于足量的水中,反应时斯裂的Cl-Cl键数目为NA
D. 标准状况下,11.2LCH3CH2OH中含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二元弱酸 H2Y 溶液中滴加 KOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如图所示,下列有关说法错误的是

A. 曲线 M 表示 pH与![]() 的变化关系
的变化关系
B. Ka2(H2Y)=10-2.7
C. d 点溶液中: c(H+)-c(OH -)=2c(Y2-)+ c(HY-)-c(K+)
D. 交点 e 的溶液中: c(H2Y) = c(Y2-) > c(HY-)> c(H+)> c(OH -)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com