
| A.1s22s22p3 | B.1s22s22p5 |
| C.1s22s22p63s23p4 | D.1s22s22p2 |
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源:不详 题型:单选题
| A.离子半径:C3->D->B+>A2+ | B.原子序数:d>c>b>a |
| C.原子半径:A>B>D>C | D.原子的最外层电子数目:A>B>D>C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题

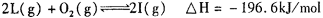 。向一个容积不变的 容器中,充入2mol L和1molO2,使之充分反应,放出的热量为Q,则Q_______196. 6kJ (填“ >”、“〈”或“=”)。
。向一个容积不变的 容器中,充入2mol L和1molO2,使之充分反应,放出的热量为Q,则Q_______196. 6kJ (填“ >”、“〈”或“=”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
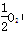 (g)===FeO(s) ΔH=-272.0 kJ·mol-1
(g)===FeO(s) ΔH=-272.0 kJ·mol-1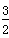 O2(g)===X2O3(s) ΔH=-1 675.7 kJ·mol-1
O2(g)===X2O3(s) ΔH=-1 675.7 kJ·mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.最易失去的电子能量最高 | B.电离能最小的电子能量最高 |
| C.p轨道电子能量一定高于s轨道电子能量 | D.在离核最近区域内运动电子能量最低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:As>Cl>P | B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- | D.酸性:H3AsO4>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第2周期 | | | | ⑥ | | ⑦ | | |
| 第3周期 | ① | ③ | ⑤ | | ⑧ | | ⑨ | ⑩ |
| 第4周期 | ② | ④ | | | | | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com