
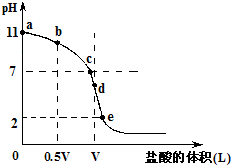
常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图像回答下列问题:
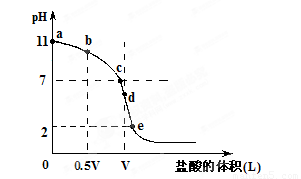
(1)氨水的电离方程式为 ,该温度时氨水的电离平衡常数K= 。
(2)比较b、c、d三点时的溶液中,水电离的c(OH-)大小顺序为 。
(3)滴定时,由b点到c点的过程中,下列各选项中数值保持不变的有 。
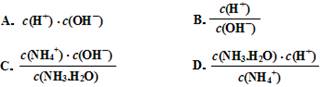
(4)根据以上滴定曲线判断下列说法正确的是(溶液中N元素只存在NH4+和NH3.H2O两种形式) 。
A.点b所示溶液中:c(NH4+)+c(H+)=c(NH3.H2O)+c(OH-)
B.点c所示溶液中:c(Cl-)=c(NH3.H2O)+c(NH4+)
C.点d所示溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.滴定中可能有:c(NH3.H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)
(5)滴定过程中所用盐酸的pH= ,d点之后若继续加入盐酸至图像中的e点(此时不考虑NH4+水解的影响),则e点对应的横坐标为 。
(1)NH3.H2O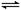 NH4++OH-(1分) 10-5(1分)
NH4++OH-(1分) 10-5(1分)
(2)d>c>b(2分) (3)ACD(3分) (4)D(2分) (5)1(2分) 11V/9(2分)
【解析】(1)一水合氨是弱电解质,存在电离平衡,方程式为NH3.H2O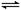 NH4++OH-。根据图像可知,0.1molL氨水中OH-浓度是0.001mol/L,所以电离平衡常数=
NH4++OH-。根据图像可知,0.1molL氨水中OH-浓度是0.001mol/L,所以电离平衡常数=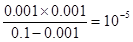 。
。
(2)当二者恰好反应时,溶液显酸性,所以bc两点氨水过量,抑制水的电离,d点恰好反应。水解促进水的电离。由于c点氨水的浓度小,所以b点抑制的程度大于c点,即水电离的c(OH-)大小顺序为d>c>b。
(3)A表示水的离子积常数,C表示氨水的电离平衡常数,均是不变的。水的离子积常数除以氨水的电离平衡常数即得到D,所以D中也不变的。由b点到c点的过程中,氢离子浓度增大,OH-浓度,所以选项C中是增大的。答案选ACD。
(4)b点氨水过量,溶液显碱性,根据电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-)可知,选项A不正确。C点显中性,题意根据电荷守恒可知,c(Cl-)=c(NH4+),选项B不正确。D点恰好反应时,显酸性,应该是c(Cl-)>c(NH4+)>c(H+)>c(OH-),所以选项C也不正确。当氨水过量时,选项D是可以正确的,答案选D。
(5)恰好反应时,消耗盐酸的体积也是VL,所以盐酸的浓度也是0.1mol/L,因此pH=1。e点对应的pH=2,所以溶液中氢离子的浓度是0.01mol/L,则有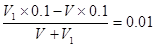 ,解得V1=11V/9。
,解得V1=11V/9。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
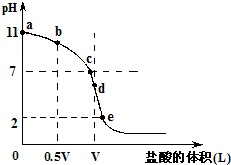 常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象回答下列问题:
常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象回答下列问题:| c(H+) |
| c(OH-) |
| c(NH4+)?c(OH-) |
| c(NH3H2O) |
| c(NH3H2O)?c(H+) |
| c(NH4+) |
| 11V |
| 9 |
| 11V |
| 9 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都七中高二下学期期中考试化学试卷(带解析) 题型:填空题
常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图像回答下列问题: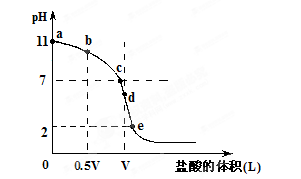
(1)氨水的电离方程式为 ,该温度时氨水的电离平衡常数K= 。
(2)比较b、c、d三点时的溶液中,水电离的c(OH-)大小顺序为 。
(3)滴定时,由b点到c点的过程中,下列各选项中数值保持不变的有 。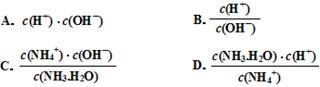
(4)根据以上滴定曲线判断下列说法正确的是(溶液中N元素只存在NH4+和NH3.H2O两种形式) 。
| A.点b所示溶液中:c(NH4+)+c(H+)=c(NH3.H2O)+c(OH-) |
| B.点c所示溶液中:c(Cl-)=c(NH3.H2O)+c(NH4+) |
| C.点d所示溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.滴定中可能有:c(NH3.H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| c(H+) |
| c(OH-) |
| c(NH4+)?c(OH-) |
| c(NH3H2O) |
| c(NH3H2O)?c(H+) |
| c(NH4+) |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都七中高二(下)期中化学试卷(解析版) 题型:解答题
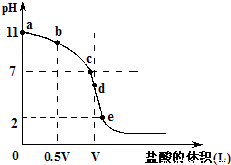 常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象回答下列问题:
常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象回答下列问题: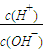 C.
C.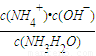 D.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com