
【题目】有下列六种转化途径,某些反应条件和产物已省略,下列有关说法正确的是( )
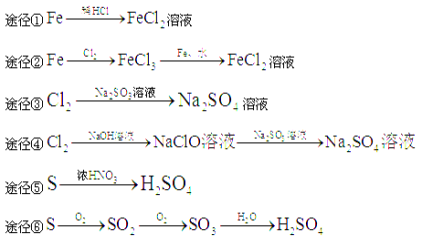
A.由途径①和②分别制取1molFeCl2,理论上各消耗1molFe,各转移2mole-
B.由途径③和④分别制取1 mol Na2SO4,理论上各消耗1 mol Cl2,各转移2mol e-
C.由途径⑤和⑥分别制取1 mol H2SO4,理论上各消耗1mol S,各转移6mol e-
D.以上说法都不正确
【答案】C
【解析】
试题分析:A、①根据元素守恒,生成1molFeCl2,消耗1molFe,转移电子物质的量为2mol,②发生反应2Fe+3Cl2=2FeCl3,Fe+2FeCl3=3FeCl2,生成1molFeCl2,消耗n(Fe)=1/3mol,n(FeCl3)=2/3mol,根据第一个反应方程式,消耗n(Fe)=n(FeCl3)=2/3mol,因此总消耗n(Fe)=1/3+2/3=1mol,转移电子物质的量为1×3/3mol+1×2/3mol=5/3mol,故错误;B、③Cl2+Na2SO3+H2O=Na2SO4+2HCl,生成1molNa2SO4,消耗1molCl2,转移电子物质的量2mol,④Cl2+2NaOH=NaCl+NaClO+H2O,ClO-+SO32-=SO42-+Cl-,生成1molNa2SO4,消耗氯气为1mol,转移电子物质的量为1mol+2mol=3mol,故错误;C、⑤发生反应S+6HNO3=H2SO4+NO2↑+2H2O,生成1molH2SO4,消耗1molS,转移电子6mol,⑥S+O2=SO2、2SO2+O2![]() 2SO3、SO3+H2O=H2SO4,根据硫元素守恒,生成1molH2SO4,消耗1molS,转移电子物质的量为6mol,故正确;D、根据上述分析,故错误。
2SO3、SO3+H2O=H2SO4,根据硫元素守恒,生成1molH2SO4,消耗1molS,转移电子物质的量为6mol,故正确;D、根据上述分析,故错误。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)
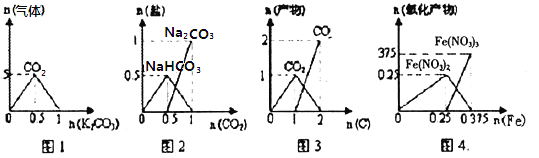
A. 图l:n(HCl)=lmol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体
B. 图2:n(NaOH)="1" mol,CO2逐步通人到NaOH溶液中反应生成的盐
C. 图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物
D. 图4:n(HNO3,)=lmol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金用途广泛,如新型储氢合金材料的研究和开发,将为氢气作为能源的实际应用起到重要的推动作用.下列材料中,不属于合金的是( )
A.青铜
B.黄铜
C.陶瓷
D.不锈钢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. C60与碳纳米管互为同素异形体
B. 最简式为CH3的有机物没有同分异构体
C. CH3C(CH3)2CH2CH3名称为2,2-二甲基丁烷
D. 核外电子总数和质子数均相同的微粒必为同种粒子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)写出图中仪器a的名称:_______________。
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为_____________,发生和收集装置为____________(填字母)。
(3)实验室用石灰石和稀盐酸反应智取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的______________端口(填“①”或“②”)通入,F中发生的化学反应方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】月球的土壤中吸附着百万吨的氦(He-3),其原子核中质子数为2、中子数为1。下列关于氦原子(He-3)的说法正确的是
A. 原子核外电子数为3 B. 相对原子质量为2
C. 原子的核电荷数为3 D. 原子结构示意图为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验题:
请从下图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积(大于25mL),并检验氯气的氧化性。
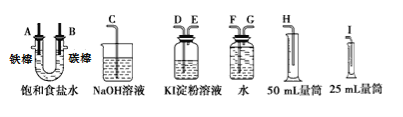
(1)A极发生的电极反应式是,B极发生的电极反应式是。
(2)设计上述气体实验装置时,各接口的正确连接顺序为:A接、接;B接、接。
(3)在实验中,盛有KI淀粉溶液的容器中发生反应的离子方程式为。
(4)已知饱和食盐水50mL(假设NaCl足量且忽略溶液体积变化),某时刻测得H2体积为16.8mL(标准状况)。此时溶液pH约为。(lg2=0.3,lg3=0.5,lg5=0.7)
(5)已知甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将甲烷燃料电池作为电源,进行上述饱和食盐水电解实验。若甲烷通入量为1L(标准状况),且反应完全,则理论上通过电解池的电量为(已知NA=6.02×1023mol-1,电子电荷为1.60×10-19C,列式表示即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶液的质量分数为b%;浓度不等的两种氨水等质量混合时,其溶质的质量分数为a%,而等体积混合后,溶液的质量分数为c%,那么a、b、c数值的关系是( )
A.a>b>c B.b>a>c C.c>b>a D.c>a>b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com