
分析 在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里和熔融状态下都不导电的化合物是非电解质,含有自由移动电子或离子的物质能导电.
解答 解:①干燥的食盐晶体不能导电,熔融状态下和溶于水中均能导电,属于电解质;
②液态氯化氢不能导电,溶于水能导电,属于电解质;
③水银能导电,属于金属单质,既不是电解质也不是非电解质;
④蔗糖不能导电,属于非电解质;
⑤纯硫酸不能导电,溶于水能导电,属于电解质;
⑥KNO3溶液能导电,属于混合物,既不是电解质也不是非电解质,
故答案为:(1)③⑥;(2)①②⑤;(3)④.
点评 本题考查了电解质和非电解质的判断,根据概念来分析解答即可,注意电解质与非电解质均为化合物,单质与混合物既不是电解质也不是非电解质,为易错点.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:解答题
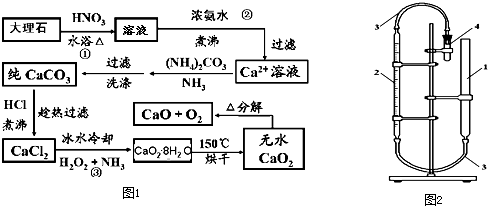
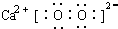 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | V正减小,V逆增大 | B. | V正增大,V逆减小 | C. | V正V逆都增大 | D. | V正V逆都减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol•L-1Na2SO4溶液中Na+个数为2NA | |
| B. | 18g水含有电子数为10NA | |
| C. | 标准状况下,22.4LH2约含有2NA个H | |
| D. | 11.2LH2一定含有NA个H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分离花生油和NaCl溶液混合液,选④ | B. | 用CC14提取碘水中的碘,选③ | ||
| C. | 用NaOH溶液吸收CO中混有的CO2选⑤ | D. | 粗盐提纯,选①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol•L-1 | B. | 7.8mol•L-1 | C. | 8mol•L-1 | D. | 1.9mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能电离出氢离子的化合物叫做酸 | |
| B. | 能电离出氢氧根离子的化合物叫做碱 | |
| C. | 盐电离出的阳离子只能是金属阳离子 | |
| D. | 由金属离子和酸根离子组成的化合物属于盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3、NH3的水溶液均能导电,所以均是电解质 | |
| B. | 蔗糖、酒精在水溶液中和熔融态时均不导电,所以它们是非电解质 | |
| C. | 液态硫酸、固态硫酸钡不能导电,所以二者均不是电解质 | |
| D. | 钢铁、石墨均导电,所以它们是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素是构成人体细胞和组织的重要材料 | |
| B. | 维生素能为人体提供能量 | |
| C. | 维生素调节新陈代谢、预防疾病和维持身体健康 | |
| D. | 维生素都溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com