
分析 (1)不能确定金属是否完全反应,需要知道盐酸的物质的量浓度;
(2)讨论过量问题进行解答,若盐酸足量,Mg完全反应,根据Mg计算氢气体积,若Mg有剩余,盐酸不足,根据盐酸计算氢气的体积,根据Mg与盐酸恰好反应确定盐酸浓度.
解答 解:(1)不能确定金属是否完全反应,需要知道盐酸的物质的量浓度amol•L-1,
故答案为:盐酸的物质的量浓度amol•L-1;
(2)0.48g Mg的物质的量=$\frac{0.48g}{24g/mol}$=0.02mol,由Mg+2HCl=MgCl2+H2↑,可知Mg与HCl恰好时,n(HCl)=0.02mol×2=0.04mol,c(HCl)=$\frac{0.04mol}{0.01L}$=4mol/L,
当c(HCl)≥4mol•L-1时,盐酸足量,Mg完全反应,则n(H2)=n(Mg)=0.02mol,故V(H2)=0.02mol×22.4L/mol=0.448L;
当c(HCl)<4mol•L-1时,Mg有剩余,盐酸不足,n(H2)=$\frac{1}{2}$n(HCl)=0.01L×amol/L=0.005a mol,故V(H2)=0.005 amol×22.4L/mol=0.112 aL,
故答案为:当c(HCl)≥4mol•L-1时V(H2)=0.448L;当c(HCl)<4mol•L-1时,V(H2)=0.112aL.
点评 本题考查化学方程式的有关计算,侧重考查过量计算,难度不大,根据恰好反应确定盐酸的浓度.


科目:高中化学 来源: 题型:选择题
| A. | SO2和SiO2 | B. | CO2和HClO | C. | NaCl和HCl | D. | CCl4和KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | a 是氧气,b 是甲醇 | |
| B. | 质子从 N 电极区穿过质子交换膜移向 M 电极区 | |
| C. | 正极反应为:O2+2H2O+4e-═4OH- | |
| D. | 当电路中有 3mole-转移时,电池中n(H+)变化为 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 | |
| B. | NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 | |
| C. | 在同一能级上运动的电子,其运动状态可能相同 | |
| D. | 若ABn的中心原子A上没有未用于形成共价键的孤对电子,当n=3,则分子结构为三角锥形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2:1 | B. | 6:1:2 | C. | 7:1:3 | D. | 7:4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
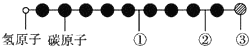 据报道,近年来发现了一种新的星际分子,其分子模型如下图所示(图中球与球之间的连线表示化学键,如单键、双键或叁键等,颜色相同的球表示同一种原子).下列对该星际分子的说法中正确的是( )
据报道,近年来发现了一种新的星际分子,其分子模型如下图所示(图中球与球之间的连线表示化学键,如单键、双键或叁键等,颜色相同的球表示同一种原子).下列对该星际分子的说法中正确的是( )| A. | ①处的化学键表示碳碳双键 | B. | 此星际分子属于烷烃 | ||
| C. | ②处的化学键表示碳碳单键 | D. | ③处的原子可能是氯原子或氟原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅的化学性质稳定,常温下不与任何物质反应 | |
| B. | 硅是构成矿物和岩石的主要元素,硅元素在地壳中的含量居第一位 | |
| C. | 硅在自然界中可以以游离态存在 | |
| D. | 高纯度的单质硅被广泛用于制作计算机芯片 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
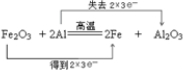 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com