
 :
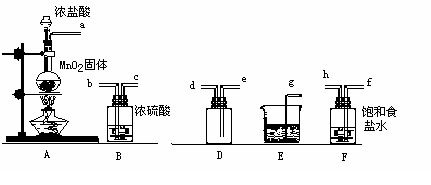
: A :MnO2+4HCl(浓)
A :MnO2+4HCl(浓) 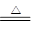 MnCl2+Cl2↑+2H2O E: Cl2+2NaOH=NaCl+NaClO+H2O 。
MnCl2+Cl2↑+2H2O E: Cl2+2NaOH=NaCl+NaClO+H2O 。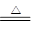 MnCl2+Cl2↑+2H2O可知,每消耗87g二氧化锰,就可以生成22.4L标准状况下的氯气,所以8.7g二氧化锰可生成2.24L氯气。40ml 10mol/L的浓盐酸的物质的量是0.4mol,根据反应式可知理论上应该生成0.1mol氯气。但由于在反应过程中盐酸的浓度逐渐降低,当降低到一定程度时,二氧化锰就不能再氧化盐酸,所以实际生成的氯气体积要小于0.1mol。
MnCl2+Cl2↑+2H2O可知,每消耗87g二氧化锰,就可以生成22.4L标准状况下的氯气,所以8.7g二氧化锰可生成2.24L氯气。40ml 10mol/L的浓盐酸的物质的量是0.4mol,根据反应式可知理论上应该生成0.1mol氯气。但由于在反应过程中盐酸的浓度逐渐降低,当降低到一定程度时,二氧化锰就不能再氧化盐酸,所以实际生成的氯气体积要小于0.1mol。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:单选题
A.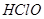 是弱酸,所以 是弱酸,所以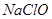 是弱电解质 是弱电解质 |
| B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体,是与水解有关 |
C.醋酸溶液和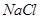 溶液均通过离子导电,是因为其溶质均为强电解质 溶液均通过离子导电,是因为其溶质均为强电解质 |
| D.22.4L氯气通入水中,理论上需要转移NA个电子(NA阿伏伽德罗常数) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯气是黄绿色,有刺激性气味的气体 | B.氯气、液氯和氯水是同一种物质 |
| C.氯气能溶于水 | D.氯气是一种有毒的气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.卤素元素都有正化合价 | B.卤素元素的单质都只具有氧化性 |
| C.卤素元素的最低化合价都是-1价 | D.卤素元素氢化物都是强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.吸水性 | B.脱水性 | C.强氧化性 | D.强氧化性和酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.“透闪石”的化学式写成氧化物的形式为:2CaO·5MgO·8SiO2·H2O |
| B.“透闪石”中Mg元素的质量分数是Ca元素质量分数的2倍 |
| C.“透闪石”的化学式写成硅酸盐的形式为:2CaSiO3·5MgSiO3·H2SiO3 |
| D.“透闪石”不耐热,也不耐酸腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HS03Cl与H20反应产物为H2S04和HCl |
| B.HSO3Cl与NaOH溶液反应生成产物只有NaS03Cl |
| C.HSO3Cl也可以用浓盐酸与浓硫酸反应制得 |
| D.O.1mol的HSO3Cl与HCl分别溶于水制得1L溶液,两者pH都等于1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.与水反应中既是氧化剂又是还原剂 | B.与NaOH反应生成溴化钠和次碘酸钠 |
| C.可作氧化剂 | D.与水反应是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com