
【题目】将一小块钠投入盛有5 mL饱和澄清石灰水的试管中,不可能观察到的现象是( )
A.钠熔成小球并在液面上到处游动
B.有气体生成
C.溶液中有银白色金属析出
D.溶液变浑浊
 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】浓盐酸和Ca(ClO)2能发生反应: Ca(ClO)2+4HCl=CaCl2+2H2O+Cl2↑,用久置漂白粉和浓盐酸反应得到的氯气中,可能含有的杂质气体是①CO2,②HCl,③H2O,④O2
A. ①②③B. ②③④C. ②③D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下: 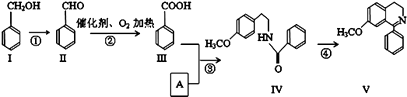
(1)Ⅱ中含氧官能团的名称 .
(2)反应②的化学方程式 .
(3)下列说法正确的是 .
A.Ⅰ和Ⅴ均属于芳香烃
B.Ⅱ能发生银镜反应
C.Ⅱ能与4molH2发生加成反应
D.反应③属于酯化反应
(4)A的结构简式 .
(5)Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种.写出满足上述条件的Ⅵ的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个完整的氧化还原反应方程式可以拆开,写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如Fe+Cu2+=Fe2++Cu,可拆写为氧化反应式:Fe-2e-=Fe2+,还原反应式:Cu2++2e-=Cu。据此,回答下列问题:
(1)将反应Zn+2H+=Zn2++H2↑拆写为两个“半反应式”:
氧化反应式:_______________________,还原反应式:_______________________。
(2)将反应2Fe3++Cu=2Fe2++Cu2+拆写为两个“半反应式”:
氧化反应式:_______________________,还原反应式:_______________________。
(3)已知某反应的两个“半反应式”为:氧化反应式CH4+10OH--8e-=![]() +7H2O,还原反应式O2+2H2O+4e-=4OH-,则氧化还原反应方程式为___________________。
+7H2O,还原反应式O2+2H2O+4e-=4OH-,则氧化还原反应方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不可能通过观察法了解的金属钠的性质是 ( )
A.钠是一种银白色金属
B.熔点为97.81 ℃,密度为0.97 g·cm-3
C.钠与H2O剧烈反应
D.钠室温下氧化和在空气中燃烧得到不同的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn还原SiCl4的反应如下:下列说法正确的是( )
SiCl4(g)+2Zn(l)Si(s)+2ZnCl2(g)△H1
SiCl4(g)+2Zn(g)Si(s)+2ZnCl2(g)△H2 .
A.Zn(l)=Zn(g)△H= ![]() (△H1﹣△H2 )
(△H1﹣△H2 )
B.用硅制作的太阳能电池是将化学能转化为电能
C.增加Zn(g)的量,△H2变大
D.以Zn片、铜片和稀硫酸构成的原电池,Zn片表面有气泡产生.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变.下列说法正确的是( ) 
A.反应体系中加入催化剂,反应速率增大,E1减小,E2增大
B.反应体系中加入催化剂,反应速率增大,△H不变
C.△H<0,反应达到平衡时,升高温度,A的转化率增大
D.△H>0,反应达到平衡时,升高温度,A的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】精确配制一定物质的量浓度的溶液通常有两种方法:直接法和标定法。直接法是准确称量一定的物质,制成一定体积的溶液;标定法则是先粗略配制一定浓度的溶液,再用已知浓度的溶液标定其浓度。对于在空气中稳定,且试剂纯度高,组成和化学式相符的物质,通常采用直接法;而对于不易提纯、组成不定或容易分解的物质,则采用标定法。
(一)用无水碳酸钠固体配制250mL 0.1000mol/L碳酸钠溶液。
(1)计算需要碳酸钠固体的质量为ag,a=__________。
(2)用分析天平准备称量质量为ag的无水碳酸钠固体,为配制所需的碳酸钠溶液还需要的玻璃仪器有:________________________________________。
(二)用浓盐酸配制250mL约0.2mol/L盐酸并标定其精确浓度。
(3)计算需要浓盐酸(质量分数为36.5%,密度为1.2g/cm3)的体积为bmL,则b=__________(计算结果保留到小数点后一位)。
(4)用量筒量取bmL浓盐酸,缓慢加入盛有(250-b)mL水的烧杯中,用玻璃棒搅拌,即得所需溶液。
(5)用酸式滴定管(注:酸式滴定管是一种可较为精确量取液体体积的量器)量取25.00mL所配盐酸溶液,放入锥形瓶,逐滴加入上述碳酸钠溶液至正好完全反应生成NaCl溶液,消耗碳酸钠溶液的体积为25.00mL,则所配制盐酸的浓度为__________。
(6)为何不用直接法配制盐酸溶液?答:________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com