
科目:高中化学 来源:不详 题型:填空题
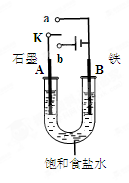
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.埋在潮湿地下的铁管道比地上的铁管道更耐腐蚀 |
| B.为保护海轮的船壳,常在船壳水线以下部分装上锌块 |
| C.在空气中,金属银的表面生成一层黑色物质 |
| D.镀层破损后,白铁皮(镀锌铁板)比马口铁(镀锡铁板)更耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铁表面镀铜,铜作阳极 |
| B.船底镶嵌锌块,锌作负极,以防船体被腐蚀 |
C.钢铁吸氧腐蚀的正极反应: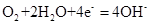 |
| D.电解精炼铜时,阳极溶解的铜与阴极析出的铜质量相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用惰性电极电解滴有紫色石蕊试液的饱和食盐水,阴极区附近溶液先变红 |
| B.镀锌的铁制品,镀层部分受损后,露出的铁表面易被腐蚀 |
| C.用惰性电极电解CuSO4溶液,在电解片刻后溶液中加Cu(OH)2固体能使CuSO4溶液恢复到电解前浓度 |
| D.配置FeCl3溶液时,可先将其溶解在盐酸中,再用蒸馏水稀释 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
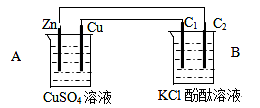
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com