
| A. | 平衡体系中氮气、氢气、氨的物质的量保持不变 | |
| B. | 平衡体系中氮气、氢气、氨的浓度保持不变 | |
| C. | 单位时间内生成的氨和分解的氨物质的量相同 | |
| D. | 单位时间内消耗的氮气和氢气与生成的氨气物质的量相同 |
分析 该反应为可逆反应,反应物不可能完全转化,当达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生改变,增大反应物浓度,可使反应速率增大,平衡向正反应方向移动.
解答 解:A.当达到平衡状态时,正逆反应速率相等,各物质的物质的量不再发生改变,故A正确;
B.当达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生改变,故B正确;反应物的浓度越大,反应速率越大,故B正确;
C.达到平衡时,正反应速率等于逆反应速率,此为平衡状态的决定性因素,故C正确;
D.正逆速率方向相同,不能判断,故D错误.
故选D.
点评 本题综合考查化学平衡知识,侧重于平衡状态的判断和平衡移动的影响,题目难度不大,注意可逆反应的特点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
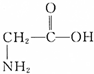 ) ④
) ④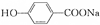 ⑤葡萄糖 ⑥乙酰水杨酸钠.
⑤葡萄糖 ⑥乙酰水杨酸钠.| A. | ①③⑤ | B. | ②④⑥ | C. | ②③④ | D. | ①⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
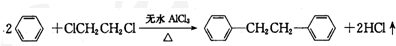
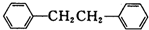 )是一种重要的有机合成中间体,实验室可用苯和1,2-二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2-二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为: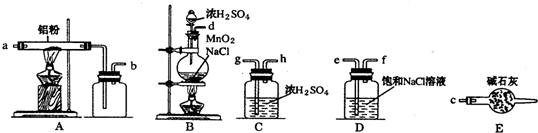

| 名称 | 相对分子质量 | 密度/(g•cm-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
| 1,2-二氯乙烷 | 99 | 1.27 | -35.3 | 83.5 | 难溶水,可溶苯 |
| 无水氯化铝 | 133.5 | 2.44 | 190 | 178(升华) | 遇水水解,微溶苯 |
| 联苄 | 182 | 0.98 | 52 | 284 | 难溶水,易溶苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
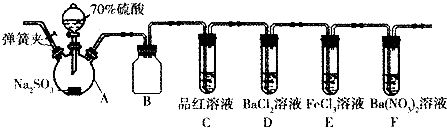
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用乙醚从黄花蒿中提取青蒿素 | B. | 由青蒿素( )合成双氢青蒿素( )合成双氢青蒿素( )的反应 )的反应 | ||
| C. | 空气净化器过滤净化空气 | D. | 消毒柜通电产生臭氧的过程 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com