
| A��ͬ�¶�ͬ���ʵ���Ũ��ʱ��HF��HCN���룬��NaF��Һ��pH��NaCN��Һ�� |
| B��0.2 mol��L-1NH4Cl��0.1 mol��L-1NaOH��Һ�������Ϻ� c(  )��c(Cl-)��c(Na+)��c(OH-)��c(H+) )��c(Cl-)��c(Na+)��c(OH-)��c(H+) |
| C�����ʵ���Ũ����ȵ�H2S��NaHS�����Һ�У� c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
D��ͬŨ�ȵ�������Һ�У���(NH4)2SO4����NH4Cl����CH3COONH4����NH3��H2O��c( )�ɴ�С��˳���ǣ��٣��ڣ��ۣ��� )�ɴ�С��˳���ǣ��٣��ڣ��ۣ��� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaHCO3��Һ�У�c(OH��)+c(HCO3��)+2c(CO32��)=c(Na+)+c(H+)+2c(H2CO3) |
| B����ˮ��NH4Cl�Ļ����Һ�У�c(NH4+)>c(Cl��) |
| C�����������Һ�м�����������õ������Ի����Һ�� c(Na+)>c(CH3COO��)>c(H+)>c(OH��) |
| D������������Һ�еμ�����������Һ�õ���pH=13�Ļ����Һ��c(Na+)=c(NO3��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2S | B��Na3PO4 | C��Na2CO3 | D��AlCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A�� +H2O +H2O NH3��H2O+H+ NH3��H2O+H+ |
B��Al3++3H2O Al��OH��3+3H+ Al��OH��3+3H+ |
C�� +2H2O +2H2O Al��OH��3+OH- Al��OH��3+OH- |
D�� +H2O +H2O H3O++ H3O++ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ��Cl-�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳�����������ֹ�ϵ��
��Cl-�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳�����������ֹ�ϵ�� )��c(H��)��c(OH-)
)��c(H��)��c(OH-) )��c(OH-)��c(H��)
)��c(OH-)��c(H��) )��c(Cl-)��c(OH-)��c(H��)
)��c(Cl-)��c(OH-)��c(H��) )��c(OH-)
)��c(OH-)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��NaHCO3���룺NaHCO3====Na++H++ |
B��H3PO4���룺H3PO4====3H++ |
C�� ˮ�⣺ ˮ�⣺ +H2O +H2O NH3��H2O+H+ NH3��H2O+H+ |
D�� ˮ�⣺ ˮ�⣺ +H2O +H2O H2CO3+2OH- H2CO3+2OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A�� ��Na+��Cl-��OH- ��Na+��Cl-��OH- | B��Al3+��Na+�� �� ��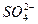 |
C��H+��Fe2+�� ��Cl- ��Cl- | D�� ��K+�� ��K+�� ��Al3+ ��Al3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pH��ȵ�CH3COONa��NaClO��NaHCO3������Һ�� c(CH3COONa) > c(NaClO) > c (NaHCO3) |
| B��Na2CO3��Һ��c��OH������c��H������c��HCO3����+ c��H2CO3�� |
| C����Ũ�ȵ�NaClO��NaHCO3�����Һ�У� c��HClO��+c��ClO����=c��HCO3����+ c��H2CO3�� |
| D��0.1 mol��L-1��KHA��Һ����pH��10��c(HA��)> c(OH��)> c(H��)> c(A2��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2CO3��Һ�У�2c(Na��)��c(CO32��)��c(HCO3��)��c(H2CO3) |
| B��NaB��Һ��pH��8��c(Na��)��c(B��)��9.9��10��7mol/L |
| C��pH��ȵĢ�NH4Cl����(NH4)2SO4����NH4HSO4������Һ�У�c(NH4��)��С˳�� �٣��ڣ��� |
| D��10mL pH��12������������Һ�м���pH��2��HA��pH�պõ���7��������Һ���V(��)��20mL |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com