
分析 (1)葡萄糖与氢氧化铜浊液反应生成葡萄糖酸和Cu2O,葡萄糖为还原剂,被氧化;
(2)用H2O2稀硫酸共同浸泡废印刷电路板可制备CuSO4;
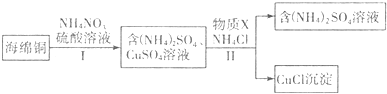
(3)海绵铜加入硫酸酸化的硝酸铵,由于酸性条件下硝酸根离子具有强氧化性,可氧化铜,加热温度不能太高,硝酸根离子可被还原生成氮氧化物,易导致环境污染,经步骤Ⅰ得到硫酸铵和硫酸铜溶液,经步骤Ⅱ可得到CuCl,反应中Cu元素被还原,则加入的X应具有还原性,可为铜或亚硫酸铵等还原性物质,注意尽量不要引入新杂质,经过滤可得到CuCl和硫酸铵溶液,以此解答该题.
解答 解:(1)葡萄糖中含有醛基,能够被新制氢氧化铜氧化为羧基,化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2$\stackrel{△}{→}$CH2OH(CHOH)4COOH+Cu2O↓+2H2O,生成葡萄糖酸和Cu2O,Cu元素化合价降低,被还原,为氢氧化铜为氧化剂,葡萄糖为还原剂,被氧化,
故答案为:还原剂;
(2)正极上是元素化合价降低,得到电子发生还原反应,将反应Cu+H2O2+H2SO4=CuSO4+2H2O,其离子方程式为:Cu+H2O2+2H+=Cu2++2H2O;
故答案为:Cu+H2O2+2H+=Cu2++2H2O;
(3)海绵铜加入硫酸酸化的硝酸铵,由于酸性条件下硝酸根离子具有强氧化性,可氧化铜,因硝酸铵易分解,则加热温度不能太高,经步骤Ⅰ得到硫酸铵和硫酸铜溶液,经步骤Ⅱ可得到CuCl,反应中Cu元素被还原,则加入的X应具有还原性,可为铜或亚硫酸铵等还原性物质,注意尽量不要引入新杂质,经过滤可得到CuCl和硫酸铵溶液,
①加热温度不能太高,硝酸根离子可被还原生成氮氧化物,易导致环境污染,0.5molNH4NO3参加反应有4mol电子转移,则N元素被还原为-3价,反应的离子方程式为4Cu+NO3-+10H+=4Cu2++NH4++3H2O;
故答案为:防止生成氮氧化物造成污染;4Cu+NO3-+10H+=4Cu2++NH4++3H2O;
②经步骤Ⅱ可得到CuCl,反应中Cu元素被还原,则加入的X应具有还原性,可为铜或亚硫酸铵等还原性物质,注意尽量不要引入新杂质,ad符合;该物质需过量以防止CuCl被氧化;
故答案为:ad;防止CuCl被氧化.
点评 本题考查物质的制备、铜的化合物的性质,侧重于学生的分析能力、实验能力和计算能力的考查,题目考查较为全面,能较好的培养学生良好的科学素养,难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | v(X)=0.005 mol•L-1•s-1 | B. | v(Z)=0.01 mol•L-1•s-1 | ||
| C. | v(Y)=0.01 mol•L-1•s-1 | D. | v(M)=0.025 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、甲苯均不能使酸性KMnO,溶液褪色 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | C4H10有三种同分异构体 | |
| D. | 石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡不会发生移动 | B. | SO3的质量分数增大 | ||
| C. | 混合气体的密度减小 | D. | 混合气体的平均相对分子质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 | |
| B. | CO2和SO2混合气体分别通入BaCl2溶液、Ba(NO3)2溶液中,最终都有沉淀生成 | |
| C. | 钠、镁着火时,不可用泡沫灭火器灭火 | |
| D. | 用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| B. |  用于分离水和苯的混合物 | |
| C. |  用于制备并收集NO2气体 | |
| D. |  用于除去碳酸氢钠固体中的少量碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒的半径:Si>Mg | B. | 氧元素不存在同素异形体 | ||
| C. | Mg的还原性强于Si | D. | 该反应是置换反应,镁元素被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com