将2.0mol SO2气体和2.0mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )
A.1.6 mol SO2+0.3 mol O2+0.4 mol SO3
B.4.0 mol SO2+1.0 mol O2
C.2.0 mol SO2+1.0 mol O2+2.0 mol SO3
D.3.0 mol SO2+0.5 mol O2+1.0 mol SO3
【答案】
分析:开始投入2.0mol SO
2气体和2.0mol SO
3气体,等效为开始投入4.0mol SO
2气体和1mol O
2气体,在恒温恒容下,平衡时SO
3的物质的量不变为n mol,说明应是完全等效平衡,按化学计量转化到左边,对应成分的物质的量相同,即满足4.0mol SO
2气体和1mol O
2气体,据此判断.
解答:解:开始投入2.0mol SO
2气体和2.0mol SO
3气体,等效为开始投入4.0mol SO
2气体和1mol O
2气体,在恒温恒容下,平衡时SO
3的物质的量不变为n mol,说明应是完全等效平衡,按化学计量转化到左边,对应成分的物质的量相同,即满足4.0mol SO
2气体和1mol O
2气体.
A、开始为1.6 mol SO
2+0.3 mol O
2+0.4 mol SO
3,转化到左边,由2SO
2(g)+O
2(g)?2SO
3(g)可知,n(SO
2)=1.6mol+0.4 mol=2mol,n(O
2)=0.3mol+

×0.4mol=0.5mol,不满足4.0mol SO
2气体和1mol O
2气体,故A错误;
B、开始为4.0 mol SO
2+1.0 mol O
2,与原平衡等效,故B正确;
C、开始为2.0 mol SO
2+1.0 mol O
2+2.0 mol SO
3,转化到左边,由2SO
2(g)+O
2(g)?2SO
3(g)可知,n(SO
2)=2mol+2 mol=4mol,n(O
2)=1mol+

×2mol=2mol,不满足4.0molSO
2气体和1molO
2气体,故C错误;
D、开始为3.0 mol SO
2+0.5 mol O
2+1.0 mol SO
3,转化到左边,由2SO
2(g)+O
2(g)?2SO
3(g)可知,n(SO
2)=3mol+1 mol=4mol,n(O
2)=0.5mol+

×1mol=1mol,满足4.0molSO
2气体和1molO
2气体,故D正确.
故选BD.
点评:本题考查化学平衡计算、等效平衡等,难度中等,清楚等效平衡规律是解题的关键.

 ×0.4mol=0.5mol,不满足4.0mol SO2气体和1mol O2气体,故A错误;
×0.4mol=0.5mol,不满足4.0mol SO2气体和1mol O2气体,故A错误; ×2mol=2mol,不满足4.0molSO2气体和1molO2气体,故C错误;
×2mol=2mol,不满足4.0molSO2气体和1molO2气体,故C错误; ×1mol=1mol,满足4.0molSO2气体和1molO2气体,故D正确.
×1mol=1mol,满足4.0molSO2气体和1molO2气体,故D正确.

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案 (2009?泰州模拟)二氧化硫是常用的化工原料,但也是大气的主要污染物.
(2009?泰州模拟)二氧化硫是常用的化工原料,但也是大气的主要污染物.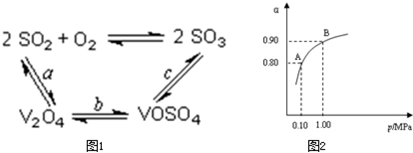
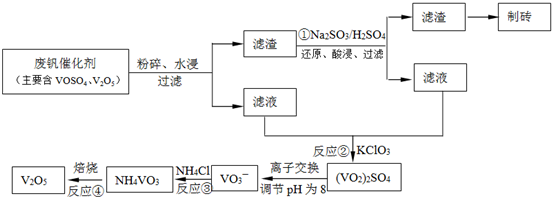
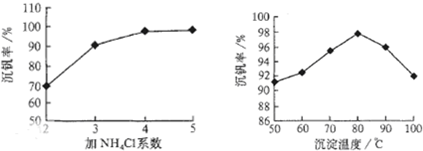

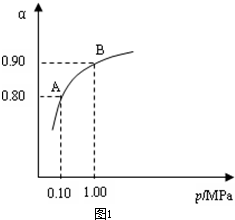 工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题:
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题: