
【题目】1000mL某待测液中除含有0.2molL﹣1的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl﹣、Br﹣、CO32﹣、HCO3﹣、SO32﹣、SO42﹣ |
现进行如下实验操作(所加试剂均过量):
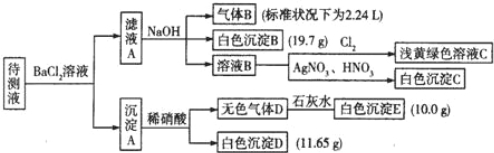
(1)写出生成白色沉淀B的离子方程式: 。
(2)若无色气体D是单一气体:
①将阴离子的物质的量浓度填入下表中(一定不存在的填“0”,不能确定的填“?”):
阴离子 | Cl﹣ | Br﹣ | CO32﹣ | HCO3﹣ | SO32﹣ | SO42﹣ |
浓度/molL﹣1 |
②判断原溶液中K+是否存在,若存在,求其物质的量浓度的最小值,若不存在,请说明理由: 。
(3)若无色气体D是混合气体,待测液中一定含有的阴离子是 。
【答案】(1)HCO3﹣+Ba2++OH﹣=BaCO3↓+H2O (2)①
阴离子 | Cl﹣ | Br﹣ | CO32﹣ | HCO3﹣ | SO32﹣ |
浓度/molL﹣1 | ? | 0 | 0.1 | 0.1 | 0 |
②存在;K+离子最小浓度为0.1mol/L;(3)CO32﹣、HCO3﹣、SO32﹣
【解析】
试题分析:根据流程图可知,加入氯化钡溶液后产生白色沉淀,向沉淀A中加入稀硝酸,部分沉淀不溶解,说明一定含有硫酸钡,则沉淀A中硫酸根离子的物质的量是11.65g÷233g/mol=0.05mol;若沉淀A中含有亚硫酸钡,则可被硝酸氧化为硫酸钡,所以不能说明原溶液中含有SO42-;沉淀部分溶解,产生的气体能使澄清石灰水变浑浊,则沉淀A中一定含有碳酸钡;说明原溶液中含有CO32-;碳酸钙沉淀的质量是10.0g,说明碳酸根离子的物质的量是10.0g÷100g/mol=0.1mol;则原溶液中一定不存在Fe3+、Ba2+;滤液A中加入氢氧化钠溶液,产生气体B,说明溶液A中含有铵根离子,则原溶液中含有铵根离子,其物质的量是2.24L÷22.4L/mol=0.1mol;滤液A还能与氢氧化钠溶液反应生成沉淀B,则该沉淀为碳酸钡沉淀,说明原溶液中一定存在HCO3-,其物质的量是19.7g÷197g/mol=0.1mol,说明原溶液中含有HCO3-的物质的量是0.1mol;向溶液B中通入氯气,得到浅黄绿色溶液,说明原溶液中不含溴离子;向溶液B中加入硝酸和硝酸银,产生白色沉淀为AgCl,但开始加入的氯化钡溶液中含有氯离子,所以不能判断原溶液中是否存在氯离子;
(1)溶液A中含有钡离子,加入过量的氢氧化钠溶液后,则氢氧根离子与碳酸氢根离子反应生成碳酸根离子和水,碳酸根离子与钡离子反应生成碳酸钡沉淀,离子方程式是HCO3﹣+Ba2++OH﹣=BaCO3↓+H2O;
(2)①若无色气体D是单一气体,说明沉淀A中不含亚硫酸钡,则溶液中不含亚硫酸根离子,所以一定含有硫酸根离子,其物质的量是0.05mol,根据以上分析可知,一定不存在的阴离子是溴离子、亚硫酸根离子;一定存在的阴离子是碳酸根离子、硫酸根离子、碳酸氢根离子,其物质的量分别是0.1mol、0.05mol、0.1mol;溶液的体积为1L,则离子的物质的量难点可以计算,其中氯离子不能确定;
②溶液中一定存在的阳离子是钠离子和铵根离子,根据电荷守恒,一定存在的阴离子的电荷总物质的量浓度为0.1×2+0.05×2+0.1=0.4mol/L,而钠离子与铵根离子的物质的量浓度之和为0.2mol+0.1mol=0.3mol/L<0.4mol/L,所以一定存在钾离子;因为氯离子不能确定,则钾离子的物质的量浓度≥(0.1×2+0.05×2+0.1-0.2-0.1)mol/L=0.1mol/L;
(3)若无色气体D是混合气体,则沉淀A中一定含有亚硫酸钡,所以待测液中一定含有的阴离子是CO32-、HCO3-、SO32-。


科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是 ( )
A.SO2、SiO2、P2O5均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.酒精、冰醋酸、草酸钾均为电解质
D.NH4SCN、SiO2、NH3·H2O均为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅的说法不正确的是
A.硅是非金属元素,但它的单质是灰黑色有金属光泽的固体
B.硅的导电性介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质反应
D.当加热到一定温度时,硅能与氧气、氯气等非金属反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 不能说明氧的非金属性比硫强的事实是( )
A.H2O的热稳定性强于H2S
B.硫化氢水溶液露置于空气中变浑浊
C.H2O是液体,H2S常温下是气体
D.氧气和氢气化合比硫和氢气化合容易
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期中的两种元素X和Y,X的原子序数大于Y,X原子的最外层电子数是内层电子总数的一半,Y的二价阴离子和Ne原子的电子层结构相同,关于X和Y形成的化合物Z的说法正确的是
A. Z是酸性氧化物 B. Z的水化物是碱
C. Z的化学式为X2Y D. Z的水化物的酸性强于硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧在烟气脱硝中的反应为2NO2(g)+O3(g) ![]() N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是
A | B | C | D |
|
|
|
|
平衡后升温, NO2含量降低 | 0~2 s内, v(O3)=0.2 mol·L-1·s-1 | v正:b点>a点 b点:v逆>v正 | 恒温, t1时再充入O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 同主族元素自上而下金属性减弱
B. 同主族元素自上而下,得电子能力增强
C. 同周期元素中ⅠA族元素的原子半径最小
D. 同周期元素中ⅦA元素气态氢化物最稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关糖类、油脂、蛋白质的说法中正确的是( )
A、都只由C、H、O三种元素组成
B、都是食物中的基本营养物质
C、都能发生水解反应
D、都属于高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com