
【题目】在25℃时,用蒸馏水稀释1mol/L的醋酸溶液至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A.![]()
B.![]()
C.![]()
D.![]() 、
、
【答案】A
【解析】解:醋酸是弱电解质,在水溶液中存在电离平衡,加水稀释促进醋酸电离,所以溶液中c(CH3COOH)减小,但醋酸电离增大程度小于溶液体积增大程度,所以溶液中c(CH3COO﹣)、c(H+)都减小,温度不变水的离子积常数不变,所以c(OH﹣)增大,
A.加水稀释促进醋酸电离,所以溶液中n(CH3COOH)减小、nc(H+)增大,因为溶液体积相同,所以 ![]() 增大,故A正确;
增大,故A正确;
B.加水稀释促进醋酸电离,所以溶液中n(CH3COOH)减小、n(H+)增大,溶液体积相等,所以 ![]() 减小,故B错误;
减小,故B错误;
C.加水稀释促进醋酸电离,所以溶液中n(CH3COOH)减小,n(CH3COO﹣)增大,溶液体积相等,所以 ![]() 减小,故C错误;
减小,故C错误;
D. ![]() =Ka , 温度不变,电离平衡常数不变,所以
=Ka , 温度不变,电离平衡常数不变,所以 ![]() 不变,故D错误;
不变,故D错误;
故选A.
醋酸是弱电解质,在水溶液中存在电离平衡,加水稀释促进醋酸电离,所以溶液中c(CH3COOH)减小,但醋酸电离增大程度小于溶液体积增大程度,所以溶液中c(CH3COO﹣)、c(H+)都减小,温度不变水的离子积常数不变,所以c(OH﹣)增大,据此分析解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
A. Mg2+、Na+、SO42-、Cl-B. Na+、Cu2+ 、SO42-、NO3-
C. Na+、K+、OH-、ClD. Ba2+、HCO3-、NO3-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl- , 消耗相同浓度的AgNO3溶液的体积之比为3:2:1,则NaCl、MgCl2、AlCl3溶液的物质的量浓度之比为( )
A.1:2:3
B.3:2:1
C.6:3:2
D.9:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是( )
A.0.2mol·L-1Na2SO4溶液中含有Na+和SO42-总物质的量为0.6mol
B.50mL 2mol·L-1的NaCl溶液和100 mL L 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C.用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol·L-1
D.10g 98%的硫酸(密度为1.84g·cm-3)与10mL 18.4mol·L-1的硫酸的浓度是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组物质所发生的变化,克服粒子间的相互作用属于同种类型的是
A. 冰和氯化铵分别受热变为气体B. 食盐和葡萄糖分别溶解在水中
C. 碘和干冰升华D. 二氧化硅和氧化钠熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,在pH=11的某溶液中,由水电离的c(OH﹣)为( )
①1.0×10﹣7 molL﹣1 ②1.0×10﹣6 molL﹣1
③1.0×10﹣3 molL﹣1 ④1.0×10﹣11 molL﹣1 .
A.③
B.④
C.①或③
D.③或④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 ![]() 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。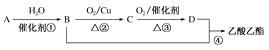
回答下列问题:
(1)写出A的电子式 , A的结构简式。
(2)B、D分子内含有的官能团分别是、(填名称)。
(3)写出下列反应的反应类型:① , ② , ④。
(4)写出下列反应的化学方程式:
①;
②;
④。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能说明刚玉(Al2O3)是一种原子晶体的是( )
①Al2O3是两性氧化物 ②硬度很大 ③它的熔点为2045℃ ④几乎不溶于水 ⑤自然界中的刚玉有红宝石和蓝宝石
A.①②③
B.②③④
C.④⑤
D.②⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com