
 (1)原子序数小于36的X、Y、Z、W四种元素,其中X是元素周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:
(1)原子序数小于36的X、Y、Z、W四种元素,其中X是元素周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:分析 (1)X是元素周期表中原子半径最小的元素,则X为H元素;Y原子基态时最外层电子数是其内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故Y为C元素;Z原子基态时2p原子轨道上有3个未成对的电子,Z的核外电子排布式为1s22s22p3,则Z为N元素;W的原子序数为29,则W为Cu.
(2)①Fe原子核外电子排布式为1s22s22p63s23p63d64s2,失去4s能级2个电子、3d能级1个电子形成Fe3+;
②Fe原子价电子数为8,CO为配体提供1对孤对电子;Fe(CO)x晶体的熔沸点比较低,易溶于非极性溶剂,应属于分子晶体;
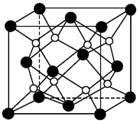
(3)晶胞中白色球数目为8,黑色球数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则白色球为钠离子、黑色球为氧离子,氧离子周围有8个钠离子,形成立方体结构;
(4)A.同周期随原子序数增大,元素第一电离能呈增大趋势,P元素原子3p能级为半满稳定状态,第一电离能高于同周期相邻元素的;
B.同周期自左而右电负性增大;
C.KCl、CaO均属于离子晶体,离子电荷越大、离子半径越小,晶格能越大,熔点越高;
D.SO2分子中S原子孤电子对数=$\frac{6-2×2}{2}$=1,价层电子对数=2+1=3,为V形结构;
E.分子晶体中,分子间作用力越强,该分子晶体的熔沸点越高,与共价键的键能无关.
解答 解:(1)X是元素周期表中原子半径最小的元素,则X为H元素;Y原子基态时最外层电子数是其内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故Y为C元素;Z原子基态时2p原子轨道上有3个未成对的电子,Z的核外电子排布式为1s22s22p3,则Z为N元素;W的原子序数为29,则W为Cu.
①Y2X2是为C2H2,碳氢原子之间形成σ键,碳碳三键中含有一个σ键,所以每个碳原子含有2个σ键,采取sp杂化,一个乙炔分子中含有3个σ键,所以1mol Y2X2含有σ键3mol或3×6.02×1023个,
故答案为:sp杂化;3mol或3×6.02×1023个;
②CO2和N2O的原子个数相等、价电子数相等,所以是等电子体,
故答案为:N2O;
(2)①Fe原子核外电子排布式为1s22s22p63s23p63d64s2,失去4s能级2个电子、3d能级1个电子形成Fe3+,基态Fe3+的M层电子排布式为3s23p63d5,
故答案为:3s23p63d5;
②Fe原子价电子数为8,CO为配体提供1对孤对电子,则8+2x=18,解得x=5;Fe(CO)x晶体的熔沸点比较低,易溶于非极性溶剂,应属于分子晶体,
故答案为:5;分子晶体;
(3)晶胞中白色球数目为8,黑色球数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则白色球为钠离子、黑色球为氧离子,氧离子周围有8个钠离子,形成立方体结构;
(4)A.同周期随原子序数增大,元素第一电离能呈增大趋势,P元素原子3p能级为半满稳定状态,第一电离能高于同周期相邻元素的,故第一电离能大小:P>S>Si,故A错误;
B.同周期自左而右电负性增大,电负性顺序:C<N<O<F,故B正确;
C.KCl、CaO均属于离子晶体,离子电荷越大、离子半径越小,晶格能越大,晶格能CaO比KCl高,所以KCl比CaO熔点低,故C正确;
D.SO2分子中S原子孤电子对数=$\frac{6-2×2}{2}$=1,价层电子对数=2+1=3,为V形结构,属于极性分子,水也是极性分子,相似相溶,二氧化硫的溶解性比二氧化碳的大,故D错误;
E.分子晶体中,分子间作用力越强,该分子晶体的熔沸点越高,与共价键的键能无关,故E错误
故选:BC.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、化学键、配合物、晶胞计算、晶体类型与性质、电离能、电负性等,是对物质结构主干知识的考查,需要显示具备扎实的基础,难度中等.


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若烃中碳、氢元素的质量分数相同,则为同系物 | |
| B. | CH2═CH2和CH2═CH-CH═CH2互为同系物 | |
| C. | 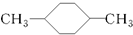 和 和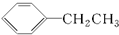 互为同分异构体 互为同分异构体 | |
| D. | 同分异构体的化学性质可能相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应是吸热反应 | |
| B. | 反应放出的热量的多少与反应物的质量和状态无关 | |
| C. | 若氢气和氧气化合是放热反应,则电解水生成氢气和氧气是吸热反应 | |
| D. | 对放热反应A+B→C+D,A、B的能量总和小于C、D的能量总和 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学平衡常数K=$\frac{{c}^{4}(C)•{c}^{2}(D)}{{c}^{3}(A)•{c}^{2}(B)}$ | |
| B. | 增大压强,平衡右移,K平衡增大 | |
| C. | B的平衡转化率是40% | |
| D. | 其他条件不变,向平衡体系中加入少量C,v正、v逆均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:2 | ||
| C. | 该有机物的分子式为C2H6 | D. | 该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放Na2CO3的一端重 | B. | 两端仍平衡 | ||
| C. | 放NaHCO3的一端重 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 分子式为C3H2O3 | |
| B. | 分子中σ键与π键个数之比为3:1 | |
| C. | 分子中既有极性键也有非极性键 | |
| D. | 分子中碳原子的杂化方式全部为sp2杂化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com