
【题目】下列各组离子在水溶液中能大量共存的是( )
A.Fe3+、OH-、CO32-B.Mg2+、Cl-、Ba2+
C.NH4+、OH-、Al3+D.Fe2+、 NO3-、H+
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】已知乙炔与苯蒸气完全燃烧的热化学方程式如下:
①C2H2(g)+![]() O2(g)―→2CO2(g)+H2O(l) ΔH=-1 300 kJ·mol-1
O2(g)―→2CO2(g)+H2O(l) ΔH=-1 300 kJ·mol-1
②C6H6(g)+![]() O2(g)―→6CO2(g)+3H2O(l) ΔH=-3 295 kJ·mol-1
O2(g)―→6CO2(g)+3H2O(l) ΔH=-3 295 kJ·mol-1
下列说法正确的是 ( )。
A. 1 mol C2H2(g)完全燃烧生成气态水时放热大于1 300 kJ
B. 1 mol C6H6(l)完全燃烧生成液态水时放热大于3 295 kJ
C. 相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多
D. C2H2(g)三聚生成C6H6(g)的过程属于放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是
A. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B. 小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O
C. NaHSO4溶液与Ba(OH)2溶液混合后呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D. 二氧化锰和浓盐酸共热:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.硫元素的同素异形体的性质相同
B.H2O2常做氧化剂,只有氧化性
C.向CaCl2溶液中通入CO2气体,有白色沉淀生成
D.汽车尾气中的NO主要是氮气和氧气在汽车汽缸中形成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1 L 0.1 mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下NH3·H2O电离平衡常数K=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如下图所示。下列叙述正确的是

A. 0.1 mol·L-1 HR溶液的pH为5
B. HR为弱酸,常温时随着氨气的通入,c(R-)/[c(OH-).c(HR)] 逐渐增大
C. 当通入0.1 mol NH3时,c(NH4+)>c(R-)>c(OH-)>c(H+)
D. 当c(R-)= c(HR)时,溶液必为中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸钾是一种白色粉末,可用作发烟剂、引火剂、氧化剂和化学分析试剂,医药工业用作解热和利尿等药剂。用PbO2来制备KClO4的工业流程如下:

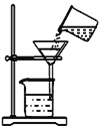
(1)如图过滤装置中有两处明显错误,一处是未用玻璃棒引流,另一处是__。
(2)写出NaClO3与PbO2反应的离子方程式_______________
(3)工业上可以利用滤液Ⅰ与KNO3发生反应制备KClO4的原因是______________
(4)用电解法也可以制备KClO4,在无隔膜、微酸性条件下,电解食盐水得到NaClO3溶液,再通过一系列转化和操作得到产品。
I.写出电解食盐水阳极电极反应式:______________________________
II.该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:准确称取5.7635 g样品溶于水中,配成250 mL溶液,从中取出25.00 mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl-,反应为:
3KClO4+C6H12O6=6H2O+6CO2↑+3KCl,加入少量K2CrO4溶液作指示剂,用0.20mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积21.50 mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
①已知:Ksp(AgCl)=1.8×l0-10,Ksp(Ag2CrO4)=1.1×10-12,若终点时c(Cl-)=1.8×10-6 mol·L-1,则此时c(CrO42-)=______________mol·L-1。
②KClO4样品的纯度为______________。(精确到0.01%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A. Ba2+、Cu2+、NO3-、SO42-B. K+、Na+、SO42-、Cl-
C. CO32-、H+、Na+、K+D. H+、Cl-、NO3-、Ag+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com