
| A、0.3mol/L |
| B、0.15mol/L |
| C、0.2mol/L |
| D、0.4mol/L |
科目:高中化学 来源: 题型:
| A、CO32-+H2O?HCO3-+OH-实验室盛放Na2CO3溶液的试剂瓶应用橡皮塞,而不用玻璃塞 |
| B、Al3++3H2O?Al(OH)3+3H+ 明矾净水 |
| C、2SbCl3+3H2O?Sb2O3+6HCl实验室可利用SbCl3的水解反应制取Sb2O3 |
| D、SnCl2+H2O?Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | ||
| Z | W |
| A、W元素的氢化物分子间有氢键 |
| B、Z和X能以共价键结合形成一种无机非金属材料 |
| C、Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 |
| D、X元素的非金属性比Y元素非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
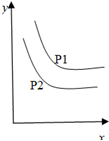 反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )| A、上述反应是放热反应 |
| B、a=b |
| C、a>b |
| D、上述反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同条件下,MnS的Ksp比CuS的Ksp大 | ||
B、该反应的平衡常数K=
| ||
| C、该反应达到平衡时c(Mn2+)=c(Cu2+) | ||
| D、往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数X<Y |
| B、原子半径X<Y |
| C、电子层数X=Y |
| D、离子半径X<Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
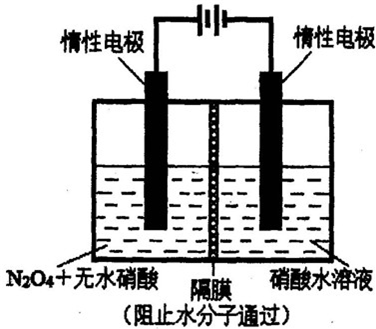 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com