
 2011��9�£��й�Ů��ѧ�������ϻ�ñ���Ϊŵ������������ꡱ����˹�˽��������й�ҽѧ������Ϊֹ��õ����缶��������������ǣ�����Ϊ�������Ϳ�űҩ--�����غ�˫�����أ������ȫ���ر��Ƿ�չ�й��ҵ��������˵�����������֪�ṹ��ͼ��ʾ��������˵����ȷ���ǣ�������
2011��9�£��й�Ů��ѧ�������ϻ�ñ���Ϊŵ������������ꡱ����˹�˽��������й�ҽѧ������Ϊֹ��õ����缶��������������ǣ�����Ϊ�������Ϳ�űҩ--�����غ�˫�����أ������ȫ���ر��Ƿ�չ�й��ҵ��������˵�����������֪�ṹ��ͼ��ʾ��������˵����ȷ���ǣ�������| A����������ά����Cһ��������ˮ���� |
| B������̼ԭ�Ӷ�������ͬһƽ���� |
| C�������ؾ���Ϊ���Ӿ��壬�仯ѧʽΪC15H22O5�����н�ǿ������ |
| D��������������θ����������ˮ�⣬��ˮ�������ʹ�Ȼ�����Һ����ɫ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ӻ������в����ܴ��ڷǼ��Լ� |
| B�����嵥�ʷ�����һ�����ڷǼ��Լ� |
| C���ڹ��ۻ������в����ܴ������Ӽ� |
| D���ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��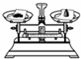 ���� |
B��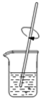 �ܽ� |
C��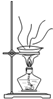 ���� |
D��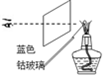 ��ɫ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��H=+88.62kJ/mol
��H=+88.62kJ/mol| A��һ�������£�1mol NBD������2 mol Br2�����ӳɷ�Ӧ |
| B������Q��������NBD�ĵ� |
| C������Q��һ��ȡ����ֻ��3�� |
| D��NBD��Q����Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������pH��7 |
| B��c��Na+��+c��H+��=c��CO32-��+c��HCO3-��+c��OH-�� |
| C��c��CO32-��+c��HCO3-��+c��H2CO3��=c��Na+�� |
| D��c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Ԫ��X�ĵ��ʼ�X��Y�γɵĻ������ܰ���ͼ��ʾ�Ĺ�ϵ����ת��������m��n���Ҿ�Ϊ��������������˵����ȷ���ǣ�������
Ԫ��X�ĵ��ʼ�X��Y�γɵĻ������ܰ���ͼ��ʾ�Ĺ�ϵ����ת��������m��n���Ҿ�Ϊ��������������˵����ȷ���ǣ�������| A����XΪFe��Y��ΪCl��Br��I�� |
| B��Xһ��Ϊ����Ԫ�� |
| C����XΪFe��Yֻ��ΪCl |
| D��X��Y���ܾ�Ϊ�ǽ���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��5e- |
| B��6e- |
| C��10e- |
| D��12e- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com