
M是原子序数<30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于电子半充满状态。
(1)M原子的外围电子排布式为_____________________,在周期表中属于???? 区元素。
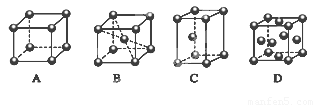
(2)M的堆积方式属于钾型,其晶胞示意图为______(填序号)。
(3)MCl3·6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3,B、[M(H2O)5Cl]Cl2·H2O和C、[M(H2O)4Cl2]Cl·2H2O。为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.010 mol MCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为_______________ (填A或B或C)。
(4) MO2Cl2常温下为暗红色液体,熔点-96.5℃,沸点117℃,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①固态MO2Cl2属于________晶体;
②CS2中碳原子和丙酮(CH3COCH3)羰基中的碳原子分别采取的杂化方式为______杂化和________杂化。
(5)+3价M的配合物K[M(C2O4)2(H2O)2]中,配体是______,与C2O42-互为等电子体的分子是(填化学式)__________。
(15分)(1)3d54s1 (2分) d(1分) (2)B(2分) (3)B(2分)
(4)①分子(2分)②sp、sp2(2分)(5)C2O42-、H2O (2分)N2O4(2分)
【解析】
试题分析:(1)M原子的最外层有空轨道,且有两个能级处于电子半充满状态,说明M为Cr,Cr原子的外围电子排布式为:3d54s1;在元素周期表位于d区。
(2)Cr的堆积方式属于钾型,K为体心立方堆积,故B型正确。
(3)取0.010 mol MCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g,沉淀为AgCl,所以Cl?的物质的量为:2.870g÷143.5g/mol=0.2mol,说明1mol该物质含有2mol Cl?,故B项正确。
(4)①MO2Cl2常温下为暗红色液体,熔点-96.5℃,沸点117℃,熔沸点较低,所以固态MO2Cl2属于分子晶体。
②CS2的结构类似于CO2,所以CS2中碳原子的杂化方式为sp杂化;丙酮(CH3COCH3)羰基中的碳原子形成了3个σ键,无孤对电子,所以为sp2杂化。
(5)根据配合物K[M(C2O4)2(H2O)2]可知配体为:C2O42-、H2O;C2O42-含有46各电子,所以与N2O4互为等电子体。
考点:本题考查电子排布、晶体堆积方式、晶体类型和杂化方式的判断、等电子体。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:2010-2011学年福建省师大附中高二下学期期中考试化学试卷 题型:单选题
X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外电子排布相同,下列说法中正确的是
| A.第一电离能X<Y | B.X的原子半径比Y小 |
| C.电负性X>Y | D.X和Y的核电荷数之差为m-n |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市延庆县高三第一次模拟理综化学试卷(解析版) 题型:填空题
X、Y、Z、L、M、N六种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是短周期原子半径最大的元素,N是地壳中含量最高的金属元素。
用化学用语回答下列问题:
(1) M在元素周期表中的位置为 ;六种元素的原子半径从大到小的顺序是
(2)Z、X两元素按原子数目比l∶3构成分子A, A的电子式为 ,Y、L两元素按原子数目比l∶2构成分子B,B中所含的化学键类型为 。
(3)硒(se)是人体必需的微量元素,已知非金属性:34Se<L。请结合原子结构解释原因 。
(4)用Y、L、M构成的正盐溶液可以清除油污,请结合离子方程式以及必要的文字解释原因 。
(5)用石墨作电极,NCl3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q。写出电解熔融Q制取N的电极方程式:阳极: ;阴极: 。
查看答案和解析>>
科目:高中化学 来源:2013届河北省高二下学期期中考试化学试卷(解析版) 题型:选择题
X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外排布相同,下列说法中正确的是( )
A.X的原子半径比Y小 B.X和Y的核电荷数之差为m-n
C.电负性X>Y D.第一电离能X<Y
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省武汉市江汉区黄冈市高三上学期期末考试(理综)化学部分 题型:填空题
(14分)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的元素。
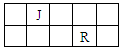
(1)元素T的名称是
(2)J和氢元素组成的化合物A每个分子由4个原子组成,已知充分燃烧a gA物质时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则A物质燃烧热的热化学方程式是
(3)工业燃烧焦炭后的尾气中含有M和R组成的气体,为了测定其含量,可以选择的试剂是
A.氢氧化钠溶液 B.硫酸酸化的高锰酸钾溶液 C.淀粉碘化钾溶液 D.溴水溶液
(4)在微电子工业中,L的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为:
(5)由L和M组成的两种价态相同的气体化合物可以相互转化,在同温同容的甲乙容器中分别加入1mol和2mol的LM2气体,分别建立平衡,则两容器中LM2的转化率比较甲 乙(<,>,=)
(6)与J同主族的另一短周期元素和M组成的化合物有很广泛的用途,请说出其主要应用,写出两种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com