
| ||
| A.该反应的氧化剂是KF,氧化产物是K |
| B.该反应能说明C的还原性大于K |
| C.电解KF溶液不可能制备金属钾 |
| D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2:1 |
科目:高中化学 来源:不详 题型:单选题
| A.锌片、铜片,稀硫酸 | B.铜片、石墨棒,乙醇 |
| C.铜片、石墨棒,稀硫酸 | D.锌片、锌片,稀硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
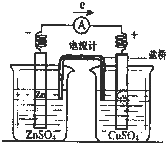
| A.铜片上有红色物质附着 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.反应中,盐桥中的K+会移向CuSO4溶液 |
| D.锌片上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 冶炼方法 | 方法 | |||||
| A | 2HgO
| 热分解法 | ||||
| B | 2Al2O3(熔融)
| 电解法 | ||||
| C | Cu2S+O2
| 热分解法 | ||||
| D | Fe2O3+2Al
| 热还原法 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
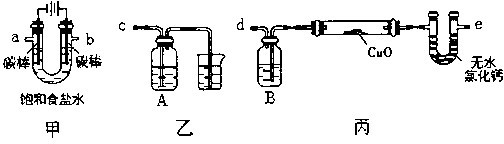
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CuSO4 | B.CuO |
| C.H2O | D.CuSO4·5H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
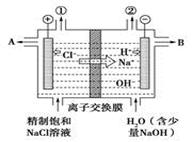
| A.转移电子0.8 mol时产生氢气8.96 L |
| B.从出口B处导出的是氢氧化钠与氯化钠的混合溶液 |
| C.装置中出口①处的气体能使湿润的淀粉碘化钾试纸变蓝 |
| D.装置中的阳离子交换膜防止产生的氯气与氢氧化钠溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com