
在密闭容器中发生如下反应:mA(g)+nB(g)⇌pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的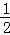 ,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是()
,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是()
A. m+n>p B. 平衡向逆反应方向移动
C. A的转化率提高 D. C的体积分数增加
考点: 化学平衡的影响因素.
专题: 化学平衡专题.
分析: mA(g)+nB(g)⇌pC(g),达到平衡后,温度不变,将气体体积压缩到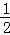 ,若平衡不移动,C的浓度为原来的2倍,当达到平衡时C的浓度为原来的1.9倍,则体积减小时平衡逆向移动,以此来解答.
,若平衡不移动,C的浓度为原来的2倍,当达到平衡时C的浓度为原来的1.9倍,则体积减小时平衡逆向移动,以此来解答.
解答: 解:mA(g)+nB(g)⇌pC(g),达到平衡后,温度不变,将气体体积压缩到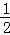 ,若平衡不移动,C的浓度为原来的2倍,当达到平衡时C的浓度为原来的1.9倍,则体积减小时平衡逆向移动,
,若平衡不移动,C的浓度为原来的2倍,当达到平衡时C的浓度为原来的1.9倍,则体积减小时平衡逆向移动,
A.体积缩小,相当于加压,平衡逆向移动,则m+n<p,故A错误;
B.由上述分析可知,平衡逆向移动,故B正确;
C.平衡逆向移动,A的转化率减小,故C错误;
D.平衡逆向移动,C的体积分数减小,但比原来的大,故D错误;
故选B.
点评: 本题考查影响平衡移动的因素,注意把握“体积压缩到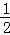 ,当达到平衡时C的浓度为原来的1.9倍”为解答的关键信息,题目难度中等.
,当达到平衡时C的浓度为原来的1.9倍”为解答的关键信息,题目难度中等.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是()
A. 制催化剂的材料 B. 半导体材料
C. 制农药的材料 D. 耐高温、耐腐蚀的合金材料
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中通入X并发生反应:2X(g)⇌Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示.下列叙述正确的是()

A. 该反应进行到M点放出的热量大于进行到W点放出的热量
B. T2下,在0~t1时间内,v(Y)=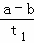 mol•L﹣1•min﹣1
mol•L﹣1•min﹣1
C. M点的正反应速率V正大于N点的逆反应速率V逆
D. M点时再加入一定量X,平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关能量转换的说法正确的是()
A. 煤燃烧是化学能转化为热能的过程
B. 化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C. 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D. 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组学习原电池知识后,决定用其原理,尝试利用铁粉、活性炭、无机盐等物质开发产品.小组提出的设想或对原理的理解不正确的是()
A. 打算制成小包装用于糕点的脱氧剂
B. 利用反应放出热量的原理制成暖宝宝
C. 调整电池结构,可降低温度,可用于延长糕点保质期
D. 正极的电极反应为:2H2O+O2+4e﹣=4OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
实验编号 反应物 催化剂
① 10mL2% H2O2溶液 无
② 10mL5% H2O2溶液 无
③ 10mL5% H2O2溶液 1mL0.1mol•L﹣1FeCl3溶液
④ 10mL5% H2O2溶液+少量HCl溶液 1mL0.1mol•L﹣1FeCl3溶液
⑤ 10mL5% H2O2溶液+少量NaOH溶液 1mL0.1mol•L﹣1FeCl3溶液
(1)催化剂能加快化学反应速率的原因是 .
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为 .
(3)实验①和②的目的是 .实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是 ).
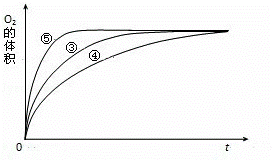
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.
分析上图能够得出的实验结论是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某结晶水的化合物的化学式为X•n H2O,X的相对分子质量为 M.若加热a g该化合物直至全部失去结晶水,得到的残渣为b g.则 n的计算式为( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
铜和镁的合金4.6g完全溶于浓硝酸,若反应后硝酸被还原只产生 2.24L的 NO2气体和1.12L的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为()
A. 9.02g B. 8.51g C. 8.00g D. 7.04g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com