ʵ���ҳ���Ũ������������̷�Ӧ��ȡ������Ũ����Ͷ������̷�Ӧ�����У�Ũ�����Ũ�Ȳ��Ͻ��ͣ�������Ũ�Ƚ����ٽ�Ũ��ʱ����Ӧֹͣ��
����һ��
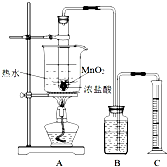
��ͬѧ����ͼװ�ã��ⶨ����Ũ�Ƚ����ٽ�Ũ��ʱ����Ӧ�����������������̽����ij�¶���Ũ������������̷�Ӧ���ٽ�Ũ�ȣ�
������A���Թ���������MnO
2�������м���10mol/L��Ũ���ᣬ�����¶�Ϊ80����з�Ӧ����ͬѧ����������ͬ����ʵ�飬�ռ����壨���������ɱ�״�������������±���
|
��һ��ʵ�� |
�ڶ���ʵ�� |
������ʵ�� |
| ��������� |
10.0mL |
10.0mL |
10.0mL |
| ��������� |
225mL |
192mL |
223mL |
�ش��������⣺
��1����д��A���Թ��ڷ�Ӧ�����ӷ���ʽ
��
��2�������װ�õ������Եķ�����
��
��3��B�м������ҺΪ
��
��4��Ϊ������������̷�Ӧ��Ũ�����ٽ�Ũ�ȣ���ͬѧ�ĵ�
��ʵ������Ӧ��ȥ�������㷴Ӧ�������ٽ�Ũ��Ϊ
��
��������
��5����ͬѧ��Ϊ��ʵ���в���֮����Ũ�����ӷ������������������ٽ�Ũ��
���ƫ�ߡ���ƫ�͡�����
��ͬѧ�����ֱ���÷�Ӧ��A�е���Һ���ⶨ������ٽ�Ũ�ȣ�
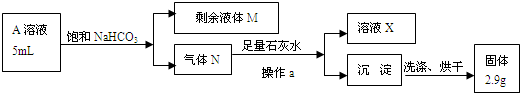
��6������ͼ���в���a��������
��
��7����д��A��Һ�е�������NaHCO3��Һ��Ӧ�����ӷ���ʽ��
��
��8�������������ݣ�Ũ��������������������ķ�Ӧ��Ũ������ٽ�Ũ��Ϊ
��

 ʵ���ҳ���Ũ������������̷�Ӧ��ȡ������Ũ����Ͷ������̷�Ӧ�����У�Ũ�����Ũ�Ȳ��Ͻ��ͣ�������Ũ�Ƚ����ٽ�Ũ��ʱ����Ӧֹͣ��
ʵ���ҳ���Ũ������������̷�Ӧ��ȡ������Ũ����Ͷ������̷�Ӧ�����У�Ũ�����Ũ�Ȳ��Ͻ��ͣ�������Ũ�Ƚ����ٽ�Ũ��ʱ����Ӧֹͣ��


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�