
① 在配制FeCl3 溶液时,常在溶液中加入一些______________以抑制其水解;其水解反应的离子方程式为_________________________。
用Al2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________。
② 比较0.1mol/L的下列各种溶液的pH大小:
CH3COONa___________NaClO;CuSO4_________KHCO3。(填“>”、“<”或“=”)
③请按顺序排列出1mol/L (NH4)2SO4溶液中各种离子浓度大小关系_______________。
科目:高中化学 来源: 题型:
香豆素是广泛存在于植物中的一类芳香族化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2。该芳香内酯A经下列步骤转变为水杨酸、乙二酸等物质。

写出化合物A的结构简式_____________________。
上述转化过程中,属于取代反应的有____个;反应步骤B→C的目的是______________。
化合物D有多种同分异构体,其中一类同分异构体是苯的二取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体(不含C-O-O-结构)共有_____种。
鉴别A、B、C三种物质,所需的试剂是________(选填编号)。
a.饱和FeCl3溶液,新制Cu(OH)2悬浊液 b.饱和FeCl3溶液,酸性KMnO4溶液
c.饱和FeCl3溶液,NaOH溶液 d.饱和FeCl3溶液,饱和NaHCO3溶液
设计合理方案,由 合成
合成 ,写出相关化学反应流程(无机试剂任取)。
,写出相关化学反应流程(无机试剂任取)。
(用合成路线流程图表示为:A B……
B…… 目标产物)。
目标产物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表述不正确的是
A.福岛核电站泄露的放射性物质131I与127I互为同位素,化学性质几乎相同
B.电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述
C.凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体
D.钠原子L层共有8种运动状态不同的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一定温度下,2X(g)+Y(g)  mZ(g) ΔH=-a kJ· mol -1
mZ(g) ΔH=-a kJ· mol -1
(a>0)。现有甲、乙两容积相等且为固定的密闭容器,保持该温度下向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时放出热量b kJ;向乙密闭容器中通入1 mol X和0.5 mol Y,达到平衡时放出热量c kJ,且b>2c。则a、b、m的值或关系正确的是
A. m=4 B. a=b C. a<b/2 D. m≤2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列混合溶液中,各离子浓度的大小顺序正确的是( )
A. 10 mL 0.1 mol ·L-1氨水与10 mL 0.1 mol ·L-1盐酸混合,
c(Cl-)>c(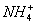 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B. 10 mL 0.1 mol ·L-1NH4Cl溶液与5 mL 0.2 mol ·L-1NaOH溶液混合,
c(Na+)=c(Cl-)>c(OH-)>c(H+)
C. 10 mL 0.1 mol ·L-1CH3COOH溶液与5 mL 0.2 mol ·L-1NaOH溶液混合,
c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D. 10 mL 0.5 mol ·L-1CH3COONa溶液与6 mL 1 mol ·L-1盐酸混合,
c(Cl-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表述中,合理的是( )
A.把FeCl3的水溶液加热蒸干可得到FeCl3固体
B.用惰性电极电解足量的CuCl2溶液时,当有0.2 mol电子转移时阳极会析出6.4g铜
C.用25 mL碱式滴定管量取15.00mL 0.1000 mol·L-1重铬酸钾溶液
D.将水加热,Kw增大,pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率
B.从海水中提镁过程中,电解熔融MgO可制备Mg
C.电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
查看答案和解析>>
科目:高中化学 来源: 题型:
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) = 2Fe(s) + 3CO(g) △H 1 = +489.0 kJ·mol-1
C(石墨) +CO2(g) = 2CO(g) △H 2 = +172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 ▲ 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K= ▲ 。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图10所示,则该反应的ΔH ▲ 0(填“>”、“<”或“=”)。


图10 图11
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图11所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ ▲ KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为 ▲ 。当氨碳比 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
▲ 。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com