
科目:高中化学 来源:2015-2016学年湖北省高二第一学期第一次月考化学试卷(解析版) 题型:选择题
甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为2CH3OH+3O2+4OH-=2CO32-+6H2O。则下列说法正确的是( )
A.电池放电时通入空气的电极为负极
B.电池放电时负极的电极反应式为CH3OH-6e-+H2O===CO2↑+6H+
C.由于CO水解显碱性,电池放电时,电解质溶液的pH逐渐增大
D.电池放电时每消耗1 mol CH3OH转移6 mol电子
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:选择题
某溶液中含有HCO3-、SO32-、CO32-、CH3COO-等4种阴离子。向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A.CH3COO- B.SO32- C.CO32- D.HCO3-
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:选择题
下列有关物质的应用与性质相对应的说法有几个
①明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
②氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜
③浓硫酸可用作干燥剂是因为其具有脱水性
④光导纤维可用作通讯材料是因为其具有导电性
⑤Mg0、Al203的熔点很高,可制作耐高温材料
⑥NaHC03能与碱反应,因此食品工业上用作焙制糕点的膨松剂
⑦Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
A.2个 B.3个 C.4个 D.5个
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上第二次段考化学试卷(解析版) 题型:填空题
(11分)将5.3 g某碱式碳酸盐固体(不含结晶水)M溶解于100 g 9.8%的稀硫酸中,充分反应后得到 224 mL CO2(标准状况)和含有MgSO4、Al2(SO4)3的溶液。向所得溶液中逐滴加入NaOH溶液,产生沉淀的质量与加入的溶质NaOH的质量关系如图所示。
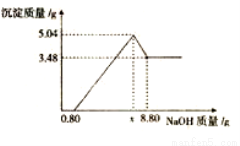
(1)由图可知,固体M与稀硫酸反应后所得溶液中除含有溶质MgSO4和Al2 (SO4)3外,还含有的溶质是 (写化学式)。
(2)加入的溶质NaOH从x g到8.8 g所发生反应的离子方程式为 。
(3)当加入溶质NaOH的质量到xg时,生成Al(OH)3的质量为 g,x= 。
(4)M的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二10月月考化学试卷(解析版) 题型:填空题
(8分) Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布为msnmpn;③R原子核外L层电子数为奇数;④Q、X原子p轨道的电子数分别为2和4。请回答下列问题:
(1)Z2+的核外电子排布式是_____________。
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的______形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是__________。
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小至大的顺序为___________ (用元素符号作答)。
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为______。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于______(填晶体类型)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二10月月考化学试卷(解析版) 题型:选择题
x、y为两种元素的原了,x的阴离了与y的阳离子具有相同的电子层结构,由此可知
A.x的原子半径大于y的原子半径 B.x的电负性大于y的电负性
C.x阴离子的半径小于y阳离子半径 D.x的第一电离能小于y的第一电离能
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期周练化学试卷(解析版) 题型:选择题
在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被水所还原的BrF3的物质的量是
A.1/3mol B.4/3mol C.1mol D.2mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年海南华侨中学高三第一次模拟考试化学试卷(解析版) 题型:选择题
用下列装置能达到有关实验目的的是
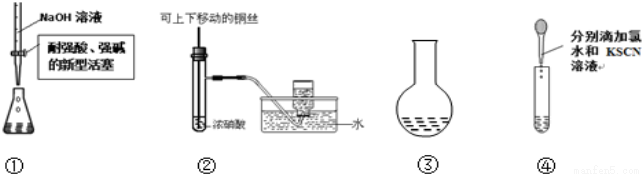
A.用①量取15.00mlNaOH溶液
B.用②制备并收集少量NO2气体
C.用③所示的仪器配制1L0.1000mol/LNaCl溶液
D.用④进行Fe2+的检验
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com