
某恒温密闭容器中,可逆反应A(s)  B+C(g) ΔH= +Q kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
B+C(g) ΔH= +Q kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1
C.若开始时向容器中加入1molB和1molC,达到平衡时放出热量等于Q kJ
D.保持体积不变,向平衡体系中加入A,平衡向正反应方向移动
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中理化学试卷(解析版) 题型:选择题
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni (s)+4CO (g)  Ni(CO)4 (g),已知该反应平衡常数与温度的关系如表:
Ni(CO)4 (g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是
A. 上述生成Ni(CO)4 (g)的反应为放热反应
B. 25℃时反应Ni(CO)4 (g)  Ni (s)+4CO (g)的平衡常数为2×10﹣5
Ni (s)+4CO (g)的平衡常数为2×10﹣5
C. 80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源:2016届山西平遥中学等重点中学高三第三次练兵化学试卷(解析版) 题型:填空题
有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D、F为常见金属元素。A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标况下的密度为0.759g/L,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应,均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。请回答下列问题:
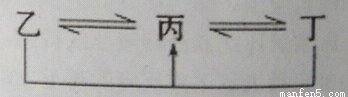
(1)单质B 的结构式: 。
(2)F元素周期表中的位置: 。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式 。
均含有D元素的乙与丁在溶液中发生反应的离子方程式 。
(4)由A、C元素组成的化合物庚和A、E元素组成的化合物辛,相对分子质量均为34.其中庚的熔沸点比辛 (填“高”或“低”),原因是 。
查看答案和解析>>
科目:高中化学 来源:2016届山西平遥中学等重点中学高三第三次练兵化学试卷(解析版) 题型:选择题
下列各项内容中,排列顺序正确的是
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②物质的熔点Li>Na>K
③微粒半径:K+>S2->F-
④单质的密度Na<K<Rb
⑤氢化物的沸点:H2Se>H2S> H2O
A.①③ B.②④ C.①② D.③⑤
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:实验题
ClO2与Cl2的氧化性相近,常温下均为气体,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。

(1)仪器C的名称是:___________。安装F中导管时,应选用图2中的:___________。(填“a”或“b”)
(2)打开B的活塞,A中氯酸钠和稀盐酸混和产生Cl2和ClO2,写出反应化学方程式:____;为使ClO2在D中被稳定剂充分吸收,可采取的措施是:__________________________。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是:_________________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为:___________,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是:______________________ 。
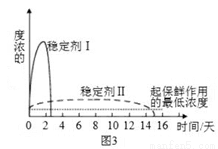
(5)已吸收ClO2气体的稳定剂Ⅰ和Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂的原因是 ________________。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古巴彦淖尔市高三上期中考试理化学试卷(解析版) 题型:选择题
下列各项表达中正确的是
A.Na2O2的电子式为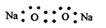
B.106的乙醇和丙醇混合液完全燃烧生成的CO2为112L (标准状况)
C.在氮原子中,质子数为7而中子数不一定为7
D.Cl-的结构示意图为
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上学期期中考试化学试卷(解析版) 题型:选择题
某稀硫酸和稀硝酸的混合溶液200ml,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解m g。向另一份中逐渐加入铁粉,产生的气体量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)下列分析或结果错误的是 ( )
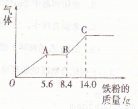
A.第二份溶液中最终溶质为FeSO4
B.原混合酸中NO3-物质的量为0.1mol
C.m值为9.6
D.H2SO4浓度为2.5mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:选择题
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com