
已知某离子的结构示意图为 ,下列说法正确的是( )
,下列说法正确的是( )
| A.该元素位于第二周期第ⅡA族 |
| B.该元素位于第二周期第Ⅷ族 |
| C.该元素位于第三周期第ⅡA族 |
| D.该元素位于第三周期0族 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
对四种元素G、L、M、R进行如下实验:
| 金属 实验 | G | L | M | R |
| 和冷水反应 | 不反应 | 慢慢反应 | 未做实验 | 未做实验 |
| 和2 mol·L-1 盐酸反应 | 溶解并放 出气体 | 溶解并 放出气体 | 不反应 | 不反应 |
| 和Rn+的 水溶液反应 | 溶解并形 成沉淀 | 未做实验 | 溶解并 形成沉淀 | 未做实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于Na+、Mg2+、Al3+三种离子,下列说法不正确的是( )
| A.核外电子层数相同 |
| B.半径大小顺序Na+<Mg2+<Al3+ |
| C.核外电子数相同 |
| D.最外层电子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列判断正确的是( )
| A.第三、四周期同主族元素的原子序数相差8 |
| B.任何原子都是核外电子层数等于该元素在周期表中的周期数 |
| C.短周期中次外层电子数是最外层电子数2倍的元素一定是非金属元素 |
| D.短周期中族序数与周期数相同的元素是H、Be |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.F、Cl、Br的最外层电子数都是7,次外层电子数都是8 |
| B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律 |
| C.卤素按F、Cl、Br、I的顺序其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用 |
| D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W是短周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是( )
| A.原子半径由小到大的顺序为X<Y<Z<W |
| B.Z的最高价氧化物能与水反应生成相应的酸 |
| C.X、Z、W最高价氧化物对应水化物酸性的强弱顺序为Z<X<W |
| D.室温下,0.1 mol/L W的气态氢化物的水溶液的pH>1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。Q元素的原子最外层电子数是其内层电子数的2倍。W、Z最外层电子数相同,Z的核电荷数是W的2倍。元素Y的合金是日常生活中使用最广泛的金属材料之一。下列说法正确的是( )
| A.原子半径的大小顺序:rX>rY>rW>rQ |
| B.X、Y的最高价氧化物的水化物之间不能反应 |
| C.Z、W最外层电子数都为6,最高化合价都为+6价 |
| D.元素Q和Z能形成QZ2型的共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是( )
| A.原子半径由小到大的顺序:X<Y<Z<W |
| B.Y单质在一定条件下可以与氧化铁发生置换反应 |
C.室温下,0.1 mol·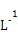 W的气态氢化物的水溶液的pH>1 W的气态氢化物的水溶液的pH>1 |
| D.Z的最高价氧化物能与水反应生成相应的酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com