
| A、HCl和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 |
| B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0 kJ?mol-1 |
| C、牺牲阳极阴极保护法是应用电解原理防止金属的腐蚀 |
| D、用洁净玻璃棒蘸取某溶液点在湿润的pH试纸上,与标准比色卡对比即可测定该溶液pH |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、氧化铝的熔点很高,可用于制作耐高温材料 |
| B、在海轮外壳上镶人锌块,可减缓船体的腐蚀速率 |
| C、电解氯化镁饱和溶液,可制得金属镁 |
| D、明矾水解形成的胶体能吸附水中悬浮物,可用于水的净化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
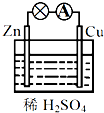
| A、锌棒为正极 |
| B、铜棒上发生还原反应 |
| C、正极反应为Cu-2e-=Cu2+ |
| D、电流从锌棒经外电路流向铜棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
32 15 |
32 15 |
| A、质子数为32 |
| B、质量数为15 |
| C、32P与33P互为同位素 |
| D、中子数为15 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打用于治疗胃溃疡病人的胃酸过多症 |
| B、工厂常用的静电除尘方法与胶体性质无关 |
| C、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板 |
| D、电解从海水中得到的氯化钠溶液可获得金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA |
| B、标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA |
| C、8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA |
| D、1 mol Na被完全氧化生成Na2O2,失去2 NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 结果分析 |
| 步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解, | 若有白色沉淀生成,说明产品中含有NaCl. |
| 步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1. | 若 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com