
【题目】下列关于胶体的说法中正确的是( )
A. 胶体外观不均匀
B. 胶体粒子不能通过滤纸
C. 胶体粒子作不停的、无秩序的运动
D. 胶体不稳定,静置后容易产生沉淀
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时,用浓度为0.1000molL﹣1的NaOH溶液分别滴定20.00mL浓度均为0.1000molL﹣1的盐酸和醋酸溶液的滴定曲线如图所示(混合溶液体积变化忽略不计).下列说法不正确的是( ) 
A.根据滴定曲线,可得Ka(CH3COOH)≈10﹣5
B.pH=7时,滴定醋酸溶液消耗的V(NaOH溶液)<20mL
C.C点溶液:c(HX)>c(X﹣)>c(Na+)>c(H+)>c(OH﹣)
D.当V(NaOH溶液)=20mL时,A点水电离出c(H+)大于B点水电离出的c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知101KPa下,1mol氢气完全燃烧生成气态水,放出244.8kJ的热量,而1mol液态水转化为气态水,需要吸收41kJ的热量.
(1)请写出氢气完全燃烧生成气态水的热化学方程式
(2)常温常压下,氢气的燃烧热为kJ/mol;
(3)阿波罗宇宙飞船使用氢氧燃料电池,在两极分别通入氢气和氧气,以KOH溶液为电解质溶液,请写出正极发生的电极反应式
(4)氢气可作为一种环保绿色能源,原因是(请写出其中两种): ①
② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑化剂(DBP)合成线路如图I: 
已知:
a.R1CHO+R2CH2CHO ![]()
![]() +H2O(R1、R2示氢原子或烃基)
+H2O(R1、R2示氢原子或烃基)
b.有机物C为含两个碳原子的烃的含氧衍生物,核磁共振氢谱图如图II.
回答下列问题:
(1)E含有的官能团是 .
(2)E→F的反应类型为
(3)符合图I转化的A的结构有种(不含立体异构).
(4)写出下列化学方程式:
①E和H2以物质的量1:1反应生成F .
②B和F以物质的量1:2合成DBP .
(5)B的同分异构体中能同时符合下列条件的有种(不含立体异构),写出其中任意两种同分异构体(填结构简式).
①不能和NaHCO3溶液反应 ②能发生银镜反应
③遇FeC13溶液显紫色 ④核磁共振氢谱显示苯环上只有一种氢原子
写出B与其中任意一种物质生成的高聚物(填结构简式).
(6)参照上述DBP合成路线,设计以苯甲醛和乙醇为起始原料制备肉桂酸( 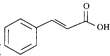 ) 的合成路线 .
) 的合成路线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁与一定浓度的稀硝酸反应时,硝酸的还原产物为NH4NO3 . 现将一定量的镁粉投入200ml 稀硝酸中,两者恰好完全反应.若向反应后的溶液中加入过量的浓NaOH溶液并微热,溶液中有白色沉淀生成,同时有氨气逸出,且逸出的氨气干燥后全部被稀硫酸吸收,稀硫酸增重0.17g.试回答下列问题:
(1)根据上述信息写出Mg和硝酸反应的化学方程式: .
(2)发生还原反应的硝酸的物质的量为mol.
(3)参加反应的镁的质量为g.
(4)原稀硝酸的物质的量浓度为 molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以2010年诺贝尔化学奖获得者的名字命名的赫克反应、根岸反应和铃木反应已成为化学家们制造复杂化学分子的“精致工具”,在科研、医药和电子等领域已经广泛应用.下例生成物就是由铃木反应合成出来的一种联苯的衍生物:![]()
下列叙述正确的是( )
A.该反应为加成反应,且原子利用率达100%
B.该联苯的衍生物属于芳香烃
C.该联苯的衍生物苯环上的一硝基取代产物有5种
D.该联苯的衍生物不可使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如图,有关它的说法正确的是( ) 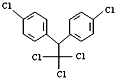
A.它属于芳香烃
B.1mol该物质能与6mol H2加成
C.分子式为C14H8Cl
D.分子中最多有22个原子共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修5:有机化学基础】端炔烃在催化剂存在下可发生偶联反应,成为Glaser反应.2R﹣C≡C﹣H ![]() R﹣C≡C﹣C≡C﹣R+H2
R﹣C≡C﹣C≡C﹣R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值.下面是利用Glaser反应制备化合物E的一种合成路线:
回答下列问题:
(1)B的结构简式为 , D的化学名称为 .
(2)①和③的反应类型分别为、 .
(3)E的结构简式为 . 用1mol E合成1,4﹣二苯基丁烷,理论上需要消耗氢气mol.
(4)化合物()也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为 .
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式 .
(6)写出用2﹣苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国的铁矿资源储量很丰富,其中以磁铁矿(主要成分Fe3O4)和赤铁矿(主要成分是Fe2O3)两种矿石为主,某炼钢厂欲用某种矿石作炼铁原料,需要对这种矿石样品分析,探究矿石中铁的价态和测定铁元素的含量,做了一些实验. I.检验矿石样品中是否有Fe2+和Fe3+
实验操作步骤:
(1)过滤操作中用到的玻璃仪器有 .
(2)检验有Fe2+和Fe3+常用的化学试剂有:KSCN溶液、新制氯水、KMnO4溶液、H2O2溶液. ①检验Fe3+选 .
②设计实验方案,证明该滤液中既有Fe2+又有Fe3+ .
(3)II.测定矿石中铁元素的含量 若上述实验中称取28g矿石样品,经过酸溶、过滤后得到200ml滤液,现取出20ml溶液装于锥形瓶中,先向锥形瓶中加入足量酸化的SnCl2溶液,充分反应后,再加入HgCl2除去过量的SnCl2 , 最后滴入20ml0.25mol/L的K2Cr2O7溶液恰好完全反应,发生的主要反应如下:2FeCl3+SnCl2=2FeCl2+SnCl4;6Fe2++Cr2O72﹣+14H+=6Fe3++2Cr3++7H2O,计算矿石样品中铁元素的质量分数是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com