
| A. | 常温下,CH3COONa和CH3COOH混合溶液中[pH=7,c(Na+)=0.1mol•L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | |
| B. | 在O.1mol•L-1Na2C03溶液中:cc(Na+)=2c(CO32-) | |
| C. | 在O.1mol•L-1NaHC03溶液中:c(HCO3-)>c(CO32-)>c(H2C03) | |
| D. | 向0.2mol•L-1NaHC03溶液中加入等体积O.1mol•L-1NaOH溶液:c(CO32-)+c(HCO3-)+c(OH-)=c(H+)+c(Na+) |
分析 A.混合液的pH=7,则c(H+)=c(OH-),根据电荷守恒可知:c(Na+)=c(CH3COO-);
B.碳酸根离子部分水解,导致碳酸根离子的浓度减小,则c(Na+)>2c(CO32-);
C.碳酸氢钠溶液呈碱性,碳酸氢根离子的水解程度大于其电离程度,则c(H2C03)>c(CO32-);
D.混合液中溶质为等体积的碳酸钠和碳酸氢钠,根据混合液中的电荷守恒判断.
解答 解:A.常温下,CH3COONa和CH3COOH混合溶液的pH=7,溶液呈中性,则c(H+)=c(OH-),根据电荷守恒可知:c(Na+)=c(CH3COO-),显性离子大于隐性离子,则溶液中离子浓度大小为:c(Na+)=c(CH3COO-)>c(H+)=c(OH-),故A正确;
B.在O.1mol•L-1Na2C03溶液中,由于碳酸根离子部分水解,则溶液中离子浓度大小为:c(Na+)>2c(CO32-),故B错误;
C.碳酸氢钠溶液中,碳酸氢根离子的水解程度大于其电离程度,则c(H2C03)>c(CO32-),溶液中正确的离子浓度大小为:c(HCO3-)>c(H2C03)>c(CO32-),故C错误;
D.0.2mol•L-1NaHC03溶液中加入等体积O.1mol•L-1NaOH溶液,根据电荷守恒可知:2c(CO32-)+c(HCO3-)+c(OH-)=c(H+)+c(Na+),故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成及盐的水解原理为解答关键,注意熟练掌握电荷守恒、物料守恒及盐的水解原理在判断离子浓度大小中的应用方法.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | Al2O3属于碱性氧化物 | |
| B. | 用烧碱溶液可以去除铁粉中混杂的少量铝粉 | |
| C. | Al(OH)3可治疗胃酸过多,说明铝元素超标对人体无影响 | |
| D. | 铝在空气中耐腐蚀,所以铝是不活泼金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯可发生加成反应 | |
| B. | 石油干馏可得到汽油、煤油等 | |
| C. | 淀粉、纤维素完全水解后的产物相同 | |
| D. | 油脂属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 131是这种碘-131的质量数 | B. | $\underset{131}{53}$I与$\underset{127}{53}$I互为同位素 | ||
| C. | 碘-131的中子数为53 | D. | 碘元素在周期表中位于第ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
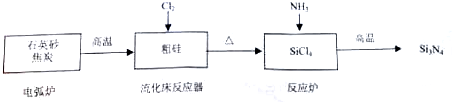
| 物质 | Si | SiCl4 | Cl2 |
| 沸点/℃ | 2355 | 57.6 | -34.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论或目的 |
| A | 向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液呈红色 | 红砖中含有氧化铁 |
| B | CO还原Fe2O3得到的黑色固体加入盐酸溶解后再加入KSCN溶液,溶液不显红色 | 黑色固体中没有Fe3O4 |
| C | 取少量Fe(NO3)2试样加水溶解,加稀H2SO4酸化,滴加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经变质 |
| D | 向某溶液中通入Cl2,然后再加入KSCN溶液变红色 | 原溶液中含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Na2O2固体中含有O22- 2NA | |
| B. | 常温常压下,3.2g CH4中含有电子2NA | |
| C. | 标准状况下,11.2L CH3CH2OH中含有分子0.5NA | |
| D. | 100mL 1mol•L-1的CH3COOH溶液中含有CH3COOH分子0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{77}^{192}$Ir原子核内含有192个质子 | |
| B. | ${\;}_{77}^{192}$Ir 和${\;}_{77}^{191}$Ir互为同位素 | |
| C. | ${\;}_{77}^{192}$Ir原子核内含有77个中子 | |
| D. | ${\;}_{77}^{192}$Ir的电子数为115 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com