
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g) CO2(g) ΔH1
CO2(g) ΔH1
C(s)+O2(g) CO(g) ΔH2
CO(g) ΔH2
②S(s)+O2(g) SO2(g) ΔH3
SO2(g) ΔH3
S(g)+O2(g) SO2(g) ΔH4
SO2(g) ΔH4
③H2(g)+O2(g) H2O(l) ΔH5
H2O(l) ΔH5
2H2(g)+O2(g) 2H2O(l) ΔH6
2H2O(l) ΔH6
④CaCO3(s) CaO(s)+CO2(g) ΔH7
CaO(s)+CO2(g) ΔH7
CaO(s)+H2O(l) Ca(OH)2(s) ΔH8
Ca(OH)2(s) ΔH8
A.① B.④ C.②③④ D.①②③
科目:高中化学 来源:2015届内蒙古赤峰市元宝山区高二上学期期末化学试卷(解析版) 题型:选择题
将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合后,溶液pH>7,以下关系式错误的是A.c(A-)> c(HA) B.c(Na+)+c(H+)= c(A-)+c(Cl-)+c(OH-)
C.c(HA)+c(A-)=0.1mol/L D.c(Na+)= c(A-)+ c(HA)
查看答案和解析>>
科目:高中化学 来源:2015届云南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
在下列给定条件的各溶液中,一定能大量共存的离子组是( )
A.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、SCN-、NO3-
B.室温下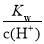 =10-13 mol·L-1的溶液中:NH4+、Mg2+、NO3-、SO42-
=10-13 mol·L-1的溶液中:NH4+、Mg2+、NO3-、SO42-
C.加入Al能放出H2的溶液中:NH4+、K+、Cl-、HCO3-
D.在H+、Na+、SO42-浓度均为0.1 mol·L-1的溶液中:K+、SiO32-、Cl-、CH3COO-
查看答案和解析>>
科目:高中化学 来源:2015届云南省云龙县高二下学期期末考试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列说法中正确的是
A.足量的Cu与含有0.2mol H2SO4的浓硫酸共热可生成SO2为0.1 NA
B.78 g 苯含有碳碳双键的数目为3NA
C.标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.1NA
D.25℃,1LpH=1的硫酸溶液中含有的H+数目为0.2NA
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步(人教选修4)1.1.1化学反应与能量的变化(解析版) 题型:选择题
根据热化学方程式:S(s)+O2(g) SO2(g) ΔH=a kJ·mol-1(a=-297.2)。分析下列说法,其中不正确的是( )
SO2(g) ΔH=a kJ·mol-1(a=-297.2)。分析下列说法,其中不正确的是( )
A.S(s)在O2(g)中燃烧的反应是放热反应
B.S(g)+O2(g) SO2(g) ΔH=b kJ·mol-1,则a>b
SO2(g) ΔH=b kJ·mol-1,则a>b
C.1 mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)所具有的能量之和
D.16 g固体硫在空气中充分燃烧,可吸收148.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时(人教选修4)4.4金属的电化学腐蚀与防护(解析版) 题型:选择题
把锌片和铁片放在盛有稀食盐水和酚酞溶液的表面皿中,如下图所示。最先观察到酚酞变红现象的区域是( )
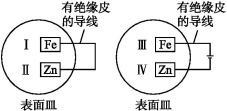
A.Ⅰ和ⅢB.Ⅰ和Ⅳ C.Ⅱ和Ⅲ D.Ⅱ和Ⅳ
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时(人教选修4)2.2影响化学反应速率的因素(解析版) 题型:填空题
用如图所示装置进行如下实验:
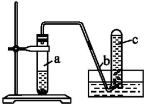
(1)在检查装置的气密性后,向试管a中加入10 mL 6 mol·L-1的稀硝酸和1 g铜片,立即用带有导管的橡皮塞塞紧试管口。请写出在试管a中有可能发生的所有反应的化学方程式 。
(2)在实验过程中常常反应开始时速率缓慢,随后逐渐加快,这是由于 ,
当反应进行一段时间后速率又逐渐减慢,原因是 。
(3)欲较快地制得NO,可采取的措施是 (填写字母序号)。
A.加热B.使用铜粉 C.稀释HNO3D.增大硝酸的浓度
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)第四章检测试卷(解析版) 题型:选择题
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为CoO2+LiC6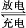 LiCoO2+C6,下列说法正确的是( )
LiCoO2+C6,下列说法正确的是( )
A.充电时,电池的负极反应为LiC6-e- Li++C6
Li++C6
B.放电时,电池的正极反应为CoO2+Li++e- LiCoO2
LiCoO2
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)4.3电解原理的应用试卷(解析版) 题型:填空题
硒是制造光电池的一种原料,人体缺少硒就会得“克山病”,从电解精炼铜的阳极泥中提取硒的流程如下:
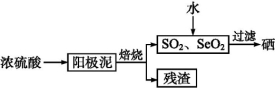
请回答下列问题:
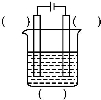
(1)实验室中电解精炼铜的简易装置如图所示,请在图中标出电极材料和电解液的名称。
(2)阳极泥中硒以Se、Ag2Se、Cu2Se等形式存在,Se与浓硫酸反应的化学方程式为 。
(3)SeO2溶于水得H2SeO3(Ka1=3.5×10-3,Ka2=5.0×10-8),亚硒酸溶液与SO2反应制硒的离子方程式为 。
电解亚硒酸溶液可制得强酸H2SeO4,则电解时的阳极反应式为 。
(4)上述硒的提取过程中存在的主要问题是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com