
【题目】A、B、C、D为四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的一种,阴离子分别是NO![]() 、SO
、SO![]() 、Cl-、CO
、Cl-、CO![]() 中的一种(离子在物质中不能重复出现)。现做如下实验:
中的一种(离子在物质中不能重复出现)。现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈蓝色;
②向①的四支试管中分别加入盐酸,B的溶液中有沉淀生成,D的溶液中有无色无味的气体逸出。
根据①②实验现象回答下列问题。
(1)写出A、C的化学式:A________________,C_______________。
(2)写出盐酸与D反应的离子方程式:_________________________。
(3)写出C与Ba(OH)2溶液反应的离子方程式:______________________。
【答案】(1)BaCl2 CuSO4;
(2)CO![]() +2H+===H2O+CO2↑;
+2H+===H2O+CO2↑;
(3)Cu2++SO![]() +Ba2++2OH-===BaSO4↓+Cu(OH)2↓
+Ba2++2OH-===BaSO4↓+Cu(OH)2↓
【解析】
试题分析:(1)①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈蓝色,则C溶液中的阳离子为Cu2+;②向①的四支试管中分别加入盐酸,B的溶液中有沉淀生成,则B中的阳离子为Ag+,由于B为可溶性盐,因此B为AgNO3;D的溶液中有无色无味的气体逸出,则D中阴离子为CO![]() ,则D为Na2CO3;故C为CuSO4,A为BaCl2;故答案:BaCl2、CuSO4;(2)盐酸与Na2CO3反应有二氧化碳气体放出,反应的离子方程式为:CO
,则D为Na2CO3;故C为CuSO4,A为BaCl2;故答案:BaCl2、CuSO4;(2)盐酸与Na2CO3反应有二氧化碳气体放出,反应的离子方程式为:CO![]() +2H+===H2O+CO2↑;(3) CuSO4与Ba(OH)2溶液反应,生成BaSO4白色沉淀和Cu(OH)2蓝色沉淀,反应的离子方程式为:Cu2++SO
+2H+===H2O+CO2↑;(3) CuSO4与Ba(OH)2溶液反应,生成BaSO4白色沉淀和Cu(OH)2蓝色沉淀,反应的离子方程式为:Cu2++SO![]() +Ba2++2OH-===BaSO4↓+Cu(OH)2↓。
+Ba2++2OH-===BaSO4↓+Cu(OH)2↓。


科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )

图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
A.图Ⅰ表示H2与O2发生反应过程中的能量变化,则H2的燃烧热△H =-241.8 kJ·mol-1
B.图Ⅱ表示反应A2 (g)+ 3B2 (g)![]() 2AB3(g),达到平衡时A2的转化率大小为:b>a>c
2AB3(g),达到平衡时A2的转化率大小为:b>a>c
C.图Ⅲ表示0.1mol MgCl2·6H2O在空气中充分加热时固体质量随时间的变化
D.图Ⅳ表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于同浓度NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时体积V(A)=V(B)=a L,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)![]() Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a L,试回答:
Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a L,试回答:
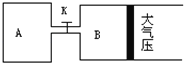
(1)B中X的转化率α(X)B为_________。
(2)A中W和B中Z的物质的量的比较:n(W)A __________________ n(Z)B(填<、>、或=)
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为_________升(用含a的代数式表示,连通管中气体体积不计)
(4)要使B容器恢复原来反应前的体积,可采取的措施是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的三种溶液:①氯化铵、②氨水、③硫酸氢铵,c(NH4+)大小顺序正确的是
A. ①>②>③ B. ③>②>① C. ②>③>① D. ③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离或提纯物质的方法正确的是( )
A.用蒸馏的方法制取蒸馏水
B.用过滤的方法除去NaCl溶液中含有的少量KNO3
C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D.用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是( )
2SO3(g)从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是( )
A .新平衡体系中,SO2和O2物质的量之比仍为2∶1
B .平衡向正反应方向移动了,原因是正反应速率增大了,逆反应速率减小了
C .新平衡体系与旧平衡体系比较,SO3的浓度肯定增大了
D .若采取的措施是缩小容器的容积,则新旧平衡中SO2和O2的转化率之比都是1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施中,不能加快化学反应速率的是
A. 将食物储存在冰箱里
B. 往H2O2溶液中加入几滴FeCl3溶液
C. 用粉末状碳酸钙代替块状碳酸钙与稀盐酸反应
D. 用稀H2SO4与锌粒反应时加入几滴CuSO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com