
【题目】下列物质中,摩尔质量最大的是( )
A. 1gCaCO3 B. 0.8mol H2SO4 C. 54g Al D. 10mL H2O
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 烧碱、纯碱、熟石灰均属于碱,稀豆浆、FeCl3溶液、蛋白质溶液均属于胶体
B. SO2、NO2、CO2等非金属氧化物都是酸性氧化物
C. 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
D. 葡萄糖溶液和淀粉溶液的本质区别是能否产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为____________。
(2)A与溴的四氯化碳溶液反应的化学方程式为____________,反应类型是____________。
(3)已知: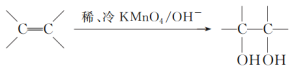 。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式___________。
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式___________。
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式__________________。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组根据镁与沸水的反应推测镁也能与饱和碳酸氢钠溶液反应.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.该兴趣小组设计了如下实验方案验证产物并探究反应原理.
实验1:用砂纸擦去镁条表面氧化膜,将其放人盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红.
(1)提出假设
该同学对反应中产生的白色不溶物作出如下假设:
假设1:可能为 .
假设2:可能为MgCO3 .
假设3:可能是碱式碳酸镁[xMgCO3yMg(OH)2]
(2)设计定性实验确定产物并验证猜测:
实验序号 | 实验 | 预期现象和结论 |
实验Ⅱ | 将实验I中收集到的气体点燃 | ① |
实验Ⅲ | 取实验I中的白色不溶物,洗涤,加入足量② | 产生气泡,沉淀全部溶解;白色不溶物可能含有MgCO3 |
实验Ⅳ | 取实验I中的澄清液,向其中加入少量CaCl2溶液 | 产生白色沉淀;溶液中存在③离子 |
(3)设计定量实验确定实验I的产物:称取实验Ⅰ中所得干燥、纯净的白色不溶物6.20g,充分加热灼烧至不再产生气体为止,并使分解产生的气体全部进入装置A(盛足量浓硫酸)和B(盛足量碱石灰)中.实验前后装置A增重0.36g,装置B增重2.64g,则白色不溶物的化学式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A. 颜色都呈红褐色
B. 能透过半透膜
C. 分散质颗粒直径都在1~100 nm之间
D. 加入浓氢氧化钠溶液都产生红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利胆解痉药“亮菌甲素”跟(CH3)2SO4反应可以生成A,二者的结构简式如图. 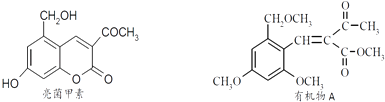
(1)“亮菌甲素”的分子式为: , 1mol“亮菌甲素”跟溴水反应时最多消耗mol Br2;能发生水解反应的官能团名称是 , 能发生还原反应的官能团名称是
(2)有机物A能发生如下转化,其中G分子中的碳原子在一条直线上. 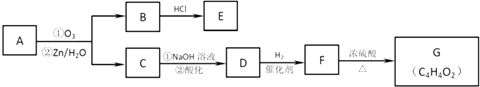
信息提示:i. ![]()
ii.R﹣O﹣CH3 ![]() R﹣OH(R为脂肪烃或芳香烃基)
R﹣OH(R为脂肪烃或芳香烃基)
①B→E的化学方程式是: .
②G的结构简式是: .
③H是G的一种同分异构体,可以发生水解反应,写出其结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )
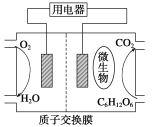
A.该电池能够在高温下工作
B.电池的负极反应式为C6H12O6+6H2O-24e-===6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体![]() L
L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,在体积相等的三个恒容器闭容器中发生可逆反应:2NH3(g)![]() N2(g)+3H3(g) ΔH=+92.4 kJ/mol。
N2(g)+3H3(g) ΔH=+92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
容器 编号 | 起始时各物质物质的量/mol | 平衡时反应中 的能量变化 | ||
NH3 | N2 | H2 | ||
① | 2 | 0 | 0 | 吸收热量a kJ |
② | 0 | 1 | 3 | 放出热量b kJ |
③ | 4 | 0 | 0 | 吸收热量c kJ |
下列叙述正确的是( )
A.热量关系:a=b
B.①②③反应的平衡常数:③>①>②
C.达平衡时H2的体积分数:①>③
D.①中的密度不再改变时说明反应已达到平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com