
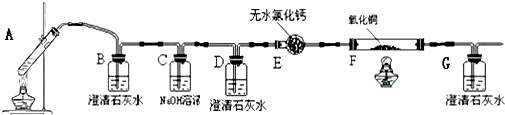
分析 (1)在后面的试验中要验证CO的存在,需要用NaOH溶液把二氧化碳除掉,装置E是吸收气体中水蒸气;
(2)乙二酸(俗名草酸)晶体受热分解,生成产物中有CO2和CO,H2O;
(3)①利用二氧化碳能使澄清石灰水变浑浊的性质来检验;
②利用CO和CuO反应生成二氧化碳的性质,来检验二氧化碳的存在,从而证明CO的存在;
(4)CO是大气污染物,需要吸收完全,不能直接排向空气中,草酸和氢氧化钙反应也生成白色沉淀.
解答 解:(1)在后面的试验中要验证CO的存在,需要用NaOH溶液把乙二酸晶体受热分解生成的二氧化碳除掉,E装置中的氯化钙吸收气体中水蒸气,干燥一氧化碳;
故答案为:吸收乙二酸晶体受热分解生成的二氧化碳;干燥CO气体;
(2)乙二酸(俗名草酸)晶体受热分解,生成产物中有CO2和CO,H2O,反应的化学方程式为:H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO↑+CO2↑,
故答案为:H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO↑+CO2↑;
(3)①二氧化碳通入装置B中,澄清石灰水变浑浊,说明有二氧化碳生成;
故答案为:装置B中澄清石灰水变浑浊;
②CO和CuO反应生成二氧化碳,二氧化碳使装置G中澄清石灰水变浑浊,先验证A中产生的二氧化碳被NaOH吸收完全,即装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊;
故答案为:装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊;
(4)CO是大气污染物,需要吸收完全,不能直接排向空气中,需要在G装置后加处理尾气CO的装置,应在B前加一个除草酸的装置,因为草酸也能和澄清石灰水反应生成沉淀;
故答案为:在G装置后加燃着的酒精灯处理尾气CO,以防止其污染空气,应在B前加一个除草酸的装置,因为草酸也能和澄清石灰水反应生成沉淀;
点评 本题考查已二酸的分解、化学计算等,题目较为综合且具有一定难度,做题时注意抓住反应的现象,以此推断物质可能具有的性质.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
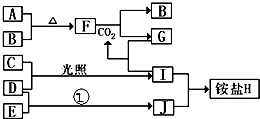 如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种固氮反应.
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种固氮反应.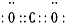 .
. 2NH3的化学方程式.
2NH3的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | T/K | 催化剂用量/g | KMnO4酸性溶液浓度mol/L | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对反应速率的影响 (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究催化剂对该反应速率的 影响; |
| ② | ||||
| ③ | 323 | |||
| ④ |
| KMnO4酸性溶液的浓度/mol•L-1 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验一:某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图:
实验一:某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中由水电离的c(H+)<10-7mol/L | |
| B. | 该溶液由0.1mol/L的CH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合而成 | |
| C. | 该溶液由V1L c mol/L的CH3COOH溶液与V2Lc mol/L的NaOH溶液混合而成,且V1<V2 | |
| D. | 在上述溶液中加入适量NaOH,可使溶液中离子浓度改变为:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  和 和 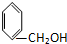 | B. | 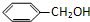 和 和 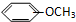 | ||
| C. | (CH3)2C(OH)CH2CH3 和CH3CH2OH | D. | CH3CH2OH 和 CH3CH2OCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 68.3% | B. | 74.2% | C. | 92.2% | D. | 78.1% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通式相同的不同有机物一定属于同系物 | |
| B. | 具有相同官能团的有机物不一定是同系物 | |
| C. | 互称为同分异构体的物质不可能具有相同的通式 | |
| D. | 互为同分异构体的物质之间物理性质一定不同,但化学性质一定相似 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com