
【题目】下列说法正确的是( ) 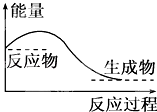
A.任何化学反应都伴随着能量的变化
B.H2O(g)═H2O(l)该过程放出大量的热,所以该过程是化学变化
C.化学反应中能量的变化都表现为热量的变化
D.对于如图所示的过程,是吸收能量的过程
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,满足下列条件的溶液一定呈酸性的是
A.pH=6的某溶液B.加酚酞后显无色的溶液
C.能与金属Al反应放出H2的溶液D.c(H+)>c(OH-)的任意水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500℃,在三个相同体积的恒容密闭容器里,分别加入对应物质,甲:2mol SO2 1mol O2乙:2mol SO2 1mol O2 1mol N2 丙:4mol SO2 2mol O2同时进行反应,开始时反应速率最大的是( )
A.甲
B.乙
C.丙
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.![]() =1012的溶液中:K+、NH4+、SO42﹣、NO3﹣
=1012的溶液中:K+、NH4+、SO42﹣、NO3﹣
B.0.1 mol/L NaAlO2溶液:Fe3+、H+、Cl﹣、SO42﹣
C.与铝反应产生大量气体的溶液:Na+、K+、CO32﹣、NO3﹣
D.使甲基橙试液显黄色的溶液:Fe2+、Mg2+、NO3﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJmol﹣1)P﹣P:198 P﹣O:360 O═O:498则反应P4(白磷)+3O2→P4O6的能量变化为( ) 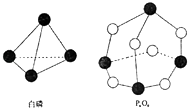
A.释放1638kJ的能量
B.吸收1638kJ的能量
C.释放126kJ的能量
D.吸收126kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.1 mol硫酸的质量为98 g·mol-1
B.硫酸的摩尔质量为98 g
C.9.8 g硫酸含有NA个硫酸分子
D.6.02×1023个硫酸分子的质量为98 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究物质的性质具有重要意义.请回答下列问题:
(1)请配平以下化学方程式:
Al+NaNO3+NaOH=NaAlO2+N2↑+H2O
若反应过程中转移5mol电子,则生成标准状况下N2的体积为L.
(2)25℃时,将a molL﹣1的氨水与0.1molL﹣1的盐酸等体积混合,当溶液中离子浓度关系满足c(NH4+)>c(Cl﹣)时,则反应的情况可能为 .
a.盐酸不足,氨水剩余b.氨水与盐酸恰好完全反应c.盐酸过量
(3)向NH4HSO4溶液中滴加少量的Ba(OH)2溶液的离子方程式 .
(4)25℃,两种酸的电离平衡常数如表.
Ka1 | Ka2 | |
H2SO3 | 1.3×10﹣2 | 6.3×10﹣8 |
H2CO3 | 4.2×10﹣7 | 5.6×10﹣11 |
①HSO3﹣的电离平衡常数表达式K= .
②0.10molL﹣1Na2SO3溶液中离子浓度由大到小的顺序为 .
③H2SO3溶液和NaHCO3溶液混合,主要反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质均为a g,将它们在氧气中完全燃烧的产物全部通入到足量的过氧化钠固体中,则过氧化钠固体增重为a g的是( )
①CO ②H2 ③CH4 ④HCHO ⑤CH3COOH ⑥HCOOH
A. ①②⑥ B. ③④⑤ C. ①②④⑤ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于容量瓶的四种叙述:①是配制准确浓度的仪器;②不宜贮藏溶液 ③不能用来加热;④使用之前要检査是否漏水。这些叙述中正确的是
A. ①②③④ B. ②③ C. ①② D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com