
【题目】实验室中固体药品应放在 瓶中,取用时块状固体用 取,粉末状固体用 取。液体药品应放在 瓶中,对于见光容易分解的溶液应放在 色的瓶中。
科目:高中化学 来源: 题型:
【题目】煤和煤制品(如水煤气、焦炭、甲醚等)已广泛应用于工农业生产中。
(1)已知:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3 kJ.mol-l
CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41.3 kJ.mol-l
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为____________,该反应在_________(填“高温”、“低温”或“任何温度”)下有利于正向自发进行。
(2)利用炭还原法可处理氮氧化物(如NO等),发生的反应为C(s)+2NO(g)![]() N2 (g)+ CO2 (g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如下表所示:
N2 (g)+ CO2 (g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如下表所示:

①10~20 min内,N2的平均反应速率可v(N2)=____________。
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是_______(填字母)。
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.遁当缩小容器的体积
(3)研究表明,反应CO(g)+H2O(g)![]() H2(g)+CO2(g)的平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)的平衡常数随温度的变化如下表所示:

若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020 mol.L-l,在该条件下达到平衡时,CO的转化率为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用1.0 mol.L-l NaOH溶液中和某浓度H2 SO4溶液时,其pH和所加NaOH溶液的体积(V)关系如图所示。则原硫酸溶液的物质的量浓度和恰好中和时溶液的总体积分别是(假设混合后溶液总体积为二者体积之和)( )

A.0.5 mol·L-1、160 mL B.1.0 mol·L-1、160 mL
C.0.5 mol·L-1、80 ml。 D.1.0 mol·L-1、80 ml。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有一学生在实验室测某溶液pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
①这种错误操作 (填“一定”/“一定不”/“不一定”)会导致实验结果有误差。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 。
(2)、用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考右图,从表中选出正确序号
序号 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 |
|
A | 碱 | 酸 | 石芯 | (乙) |
B | 酸 | 碱 | 酚酞 | (甲) |
C | 碱 | 酸 | 甲基橙 | (甲) |
D | 酸 | 碱 | 酚酞 | (乙) |
(3)、用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是 。
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证干燥的氯气无漂白性,湿润的氯气具有漂白性,某同学设计实验如下图。其中B、C、D、E、F分别盛有饱和食盐水、浓硫酸。干燥红色布条、浓硫酸、湿润红色布条。

请回答:
(1)E中浓硫酸的作用____________。
(2)将F中的湿润布条换成卷曲的细铜丝,并用酒精灯加热,可看到的现象是_____________。
(3)若用装置A制取2.24L(标况)氯气,消耗10mol/L浓盐酸的体积明显大于40mL,造成该结果的可能原因有______________。
A.浓盐酸的挥发 B.随反应进行盐酸浓度下降
C.加热时火力不够猛 D.MnO2固体过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液的pH相比较(相同温度下)( )
A.前者大 B.相等 C.后者大 D.不能肯定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组内的反应,其实质属于同一类型的是 ( )
A. 制备酚醛树脂、制取聚苯乙烯
B. 酯化反应,酯的水解
C. 制取聚丙烯、聚四氟乙烯、丁苯橡胶(单体为丁二烯和苯乙烯)
D. 乙烯水解、苯硝化反应、苯酚与浓溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂.
Ⅰ.测定中和热.
(1)写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式 (中和热数值为57.3kJ/mol):
(2)取50mL 0.5mol/L HCl溶液与50mL0.55mol/L NaOH溶液进行测定,但实验数值小于57.3kJ/mol,原因可能是 _(填序号).
A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
B.量取盐酸的体积时仰视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
D.实验装置保温、隔热效果差
Ⅱ.酸碱中和滴定.
(1)某学生用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液,选择酚酞作指示剂.实验中不必用到的是
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
(2)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________.当________时,即停止滴定.
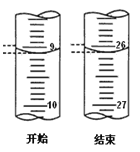
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:已知用c(HCl)=0.10 mol/L的盐酸标定25mL的氢氧化钠溶液,测得c(NaOH)______ ___mol/L
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是___ ___(填序号).
A.锥形瓶用蒸馏水洗净后没有干燥
B.碱式滴定管未用待测液润洗就直接注入待测氢氧化钠溶液
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com