
| A. | 0.01 | B. | 100 | C. | 0.1 | D. | 无法确定 |
分析 化学平衡常数指,一定温度下,可逆达到平衡,各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,故对于同一可逆反应,相同温度下,正、逆两个方向的平衡常数互为倒数,同一可逆反应,平衡常数与系数成对应幂次方关系.
解答 解:对于同一可逆反应,相同温度下,正、逆两个方向的平衡常数互为倒数,已知450℃时,反应H2(g)+I2(g)?2HI(g)的K=100,则在450℃时,反应 2HI(g)?H2(g)+I2(g)的化学平衡常数为$\frac{1}{100}$=0.01,所以在450℃时,反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)的平衡常数$\sqrt{0.01}$=0.1.
故选C.
点评 本题考查平衡常数的书写、计算等,比较基础,掌握平衡常数的书写与意义即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
 甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般采用下列反应合成甲醇CO(g)+2H2(g)?CH3OH(g)△H
甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般采用下列反应合成甲醇CO(g)+2H2(g)?CH3OH(g)△H| 温度 | 250℃ | 300℃ | 350℃ |
| K | 3.041 | 1.000 | 0.120 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有反应的反应热都可以由实验直接测定 | |
| B. | 任何化学反应都需要用活化能来引发 | |
| C. | 200°C、101KPa时,1g氢气与碘蒸气作用生成HI气体,放出7.45kJ热量,则此过程的热化学方程式可表示为:H2(g)+I2(g)=2HI(g)△H=-14.9kJ/mol | |
| D. | 没有物质的变化,就不能引发能量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3 | B. | MgSO4 | C. | Na2SO3 | D. | Ca(HCO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| C. | 在20℃,1.01×105Pa时,1 NA 个CO2分子占有的体积为22.4L | |
| D. | 1mol/L NaCl溶液中含有钠离子的个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ②③ | C. | ①③ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题


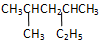 的系统命名是:2,4-二甲基己烷
的系统命名是:2,4-二甲基己烷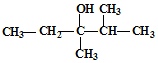 的键线式是
的键线式是
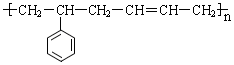 的单体结构简式为:
的单体结构简式为: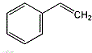 和CH2=CH-CH=CH2
和CH2=CH-CH=CH2

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加入适量铁粉的方法除去Cu(NO3)2溶液中混有的AgNO3杂质 | |
| B. | 用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 | |
| C. | 用溶解、过滤的方法分离KNO3和NaCl固体的混合物 | |
| D. | 先后添加石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com