
分析 由Cl-+Ag+═AgCl↓计算XCl2的物质的量,再由M=$\frac{m}{M}$计算其摩尔质量,摩尔质量与相对分子质量的数值相等,原子的质量数为原子的近似相对原子质量,结合该原子原子核内有12个中子,根据质子数=质量数-中子数来计算原子的质子数,利用质子数确定元素在周期表中的位置,根据物质的种类书写离子反应方程式.
解答 解:(1)由Cl-+Ag+═AgCl↓可知,n(Cl-)=n(Ag+)=0.02L×1mol/L=0.02mol,
n(XCl2)=$\frac{1}{2}$n(Cl-)=$\frac{1}{2}$×0.02mol=0.01mol,
则M(XCl2)=$\frac{0.95g}{0.01mol}$=111g/mol,
所以XCl2相对分子质量为95,
所以X的相对原子质量=95-35.5×2=24,即X的质量数为24,
质子数=质量数-中子数=24-12=12,即Z=12,A=24
故答案为:12;24;
(2)质子数是12的为镁,镁与盐酸反应的离子方程式:Mg+2H+=Mg2++H2↑,故答案为:Mg+2H+=Mg2++H2↑.
点评 本题考元素周期表的结构及应用,为高频考点,把握发生的离子反应及原子构成为解答的关键,注意分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
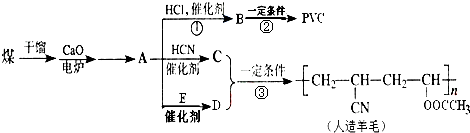
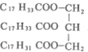 .请回答下列问题:
.请回答下列问题: (写结构简式).
(写结构简式). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下是气体,易溶于水 | |
| B. | 甲烷的一氯取代物有一种,乙烷的一氯取代物有2种 | |
| C. | 在光照条件下能与Cl2发生取代反应 | |
| D. | 在空气中不能点燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35Cl和37Cl互为同位素 | |
| B. | 元素的化学性质主要取决于核外电子数 | |
| C. | 物质之间发生化学变化时,化学键一定发生变化 | |
| D. | 熔融状态下能够导电的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 臭氧层破坏:CO2 | |
| B. | 水体富营养化:含超量氮、磷元素的物质 | |
| C. | 光化学烟雾:CO | |
| D. | 酸雨:HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,C4H10是气体 | |
| B. | C4H10与CH4互为同系物 | |
| C. | 丁烷有正丁烷与异丁烷两种同分异构体 | |
| D. | C4H10进行一氯取代后最多生成两种沸点不同的产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com