
下列说法正确的是 ( )
A.CO2的水溶液能导电,所以CO2是电解质
B.BaSO4不溶于水,其水溶液的导电能力极弱,所以BaSO4是弱电解质
C.液溴不导电,所以液溴是非电解质
D.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
Ⅰ、(7分)在一定条件下,将 2 molA 和 2 molB 混合于容积为 2L 的密闭容器中,发生如下反应:
3A ( g ) + B ( g )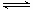 xC ( g ) + 2D ( g )。 2 min 末反应达到平衡状态时,生成 0.8molD ,同时测得 C 的浓度为 0.4 mol·L一1。请填写下列空白:
xC ( g ) + 2D ( g )。 2 min 末反应达到平衡状态时,生成 0.8molD ,同时测得 C 的浓度为 0.4 mol·L一1。请填写下列空白:
(1)x =_________;用 D 的浓度变化表示的化学反应速率为___________________
(2)A 的平衡浓度为_______________________ , B 的转化率为_____________。
(3)如果增大体系的压强,则平衡体系中 C 的体积分数将____________(填“增大”、“减小”或“不变”)。
Ⅱ、(12分)在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g)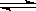 CO(g)+H2O(g)
CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,则该温度下反应
CO(g)+H2O(g)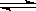 CO2(g)+H2(g)的平衡常数K2=________,
CO2(g)+H2(g)的平衡常数K2=________,
反应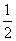 CO2(g)+
CO2(g)+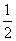 H2(g)
H2(g)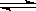
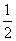 CO(g)+
CO(g)+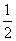 H2O(g)的平衡常数K3=________。
H2O(g)的平衡常数K3=________。
(3)已知在1 000 ℃时,该反应的平衡常数K4为1.0,则该反应为________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是________。
A.容器中压强不变 B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2 D.混合气体的平均相对分子质量不变
(5)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v(正)________v(逆)(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种非 金属元素具有相同的电子层数,它们的气态氢化物的稳定性的强弱顺序为XH3<H2Y<HZ,则三种元素的非金属性和简单阴离子的还原性强弱顺序如何?
金属元素具有相同的电子层数,它们的气态氢化物的稳定性的强弱顺序为XH3<H2Y<HZ,则三种元素的非金属性和简单阴离子的还原性强弱顺序如何?
查看答案和解析>>
科目:高中化学 来源: 题型:
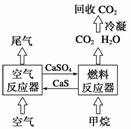 直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙。硫酸钙可在下图所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的。
直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙。硫酸钙可在下图所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的。
请回答下列问题:
(1)煤燃烧产生的烟气直接排放到空气中,引发的主要环境问题有______(填写字母编号)。
A.温室效应 B.酸雨
C.粉尘污染 D.水体富营养化
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间的二氧化碳,以增加其脱硫效率;脱硫时控制浆液的pH,此时浆液含有的亚硫酸氢钙可以被氧气快速氧化生成硫酸钙。
①二氧化碳与石灰石浆液反应得到的产物为__________。
②亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式为
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,w g某物质在足量氧气中充分燃烧,其燃烧产物立即与过量的Na2O2反应,固体质量增加w g。在①H2 ②CO ③CO和H2的混合气 ④HCHO ⑤C2H6O2中,符合题意的是 ( )
A.均不符合 B.只有①②③ C.只有④⑤ D.全部符合
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
Ⅰ.把氯气通入紫色石蕊溶液中,可以观察到的现象是:
________________________________________________________________________。
请你解释其中的原因______________________________________________________。
Ⅱ.某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。
(1)其反应原理为:(用化学方程式表示)
________________________________________________________________________。
(2)实验室配制好4.0 mol·L-1的NaOH溶液,这种溶液________L才能与2.24 L氯气(标准状况)恰好完全反应。
(3)配制480 mL 4.0 mol·L-1 NaOH溶液的实验步骤:
a.计算需要氢氧化钠固体的质量。
b.称量氢氧化钠固体。
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶。
d.用适量蒸馏水溶解称量好的氢氧化钠固体,冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1 cm~2 cm时,改用胶头滴管加蒸馏水至凹液面与刻度线相切。
①用天平称量的所需氢氧化钠固体的质量是______g。
②上述步骤的正确操作顺序是
_______________________________________________________________________。
③上述实验需要的玻璃仪器有
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( )
①苯不能使溴水褪色②苯不能使酸性高锰酸钾溶液褪色③苯在一定条件下既能发生取代 反应,又能发生加成反应④经测定,邻二甲苯只有一种结构⑤经测定,苯环上碳碳键的键长相等,都是1.40×10-10m。
A.①② B.①②③⑤ C.①②③ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
2005年诺贝尔化学奖被授予“在烯烃复分解反应研究方面作出贡献”的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如2分子烯烃RCH=CHR'用上述催化剂作用会生成两种新的烯烃RCH=CHR和R'CH=CHR'。则分子式为C4H8的烯烃中,任取两种发生“复分解反应”,生成新烯烃种类最多的一种组合中,其新烯烃的种类为( )
A.5种 B.4种 C.3 种 D.2种
查看答案和解析>>
科目:高中化学 来源: 题型:
除去括号内杂质所用试剂和方法不正确的是
A.Cu(Fe)----加盐酸,过滤;
B.乙醇(水)----加生石灰,蒸馏;
C.KNO3溶液(KCl)----降温结晶,过滤;
D.CO2(HCl)----饱和NaOH溶液,洗气。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com