
| ʵ�鲽�� | Ԥ������ͽ��� | |
| �� | ȡ��������Ư�����Թ��У���������1mol/L�����ܽ���ٽ����������嵼�����ʯ��ˮ�У� | ��1��������ʯ��ˮδ�����ǣ������1������ ��2��������ʯ��ˮ����ǣ������2��3������ |
| �� | ����ٷ�Ӧ����Թ��е���1��2��Ʒ����Һ����������ȡ�������� | ���ʵ����еģ�2���� ��1����Ʒ����ɫ�������3������ ��2����Ʒ�첻��ɫ�������2������ |
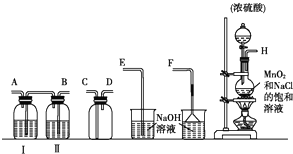
���� ��1��H�����������к���HCl��ˮ���������ñ���ʳ��ˮ��ȥHCl������Ũ���������������ȡ�����ſ������ռ����������������������Һ���ն������������ֹ��Ⱦ������������������Һ����������ֹ��������װ��������ӦΪ�����̳���
��2���ɣ�1��������֪��װ������˳�����Ӻ�ʵ��װ�ú���Ҫ���������Լ��飬Ȼ���ڿ�ʼʹ�ã�
��3����������ʯ������ȡƯ�ۣ���Ӧ�����Ȼ��ơ����������ˮ�����ݷ���ʽ��֪��Ӧ������Ϊ����������ԭ������ռһ�룬��������ת�Ƶ��ӣ�
��4����Ư�۳ɷ�ΪCaCl2��Ca��ClO��2���������������ж�����̼��ˮ��Ӧ����CaCO3�����ʣ�
����Ư�۱��ʣ�����CaCO3������������ж�����̼���ɣ���ͨ�����Ƴ���ʯ��ˮ������̼��ư�ɫ�������ɣ�����û�У�
����ٷ�Ӧ����Թ��е���1��2��Ʒ����Һ������Ʒ����Һ�Ƿ���ɫ�ж��Ƿ���Ca��ClO��2��
��� �⣺��1��H�����������к���HCl��ˮ���������ñ���ʳ��ˮ��ȥHCl������Ũ���������������ȡ�����ſ������ռ����������������������Һ���ն������������ֹ��Ⱦ������������������Һ����������ֹ��������װ��������ӦΪ�����̳�������������������ķ��������������ӣ�H��B��A��C��D��F��������ʢ�Լ�ΪŨ���ᣬ������ʢ�Լ�Ϊ����ʳ��ˮ��
�ʴ�Ϊ��C��B��
��2���ɣ�1��������֪������������������ķ��������������ӣ�H��B��A��C��D��F�����Ӻ�ʵ��װ�ú���Ҫ����װ�������ԣ�Ȼ���ڿ�ʼʹ�ã�
�ʴ�Ϊ��B��A��D��F����ֹ����������װ�������ԣ�
��3����������ʯ������ȡƯ�ۣ���Ӧ�����Ȼ��ơ����������ˮ����Ӧ����ʽΪ��2Cl2 +2Ca��OH��2 =CaCl2 +Ca��ClO��2 +2H2O�����ݷ���ʽ��֪��Ӧ������Ϊ����������ԭ������ռһ�룬������£�33.6L Cl2�μӷ�Ӧ�������ʵ���Ϊ$\frac{33.6L}{22.4L/mol}$=1.5mol����ת�Ƶ���Ϊ1.5mol��$\frac{1}{2}$��2=1.5mol��
�ʴ�Ϊ��2Cl2 +2Ca��OH��2 =CaCl2 +Ca��ClO��2 +2H2O��1.5��
��4����Ư�۳ɷ�ΪCaCl2��Ca��ClO��2���������������ж�����̼��ˮ��Ӧ����CaCO3�����ʣ���CaCl2�⣬̽������Ʒ�п��ܴ��ڵ������������ʣ�����������裺
����1����Ư��δ���ʣ�ֻ��Ca��ClO��2��
����2����Ư��ȫ�����ʣ�ֻ��CaCO3��
����3����Ư�۲��ֱ��ʣ�����CaCO3��Ca��ClO��2��
�ʴ�Ϊ��Ca��ClO��2��CaCO3��Ca��ClO��2��
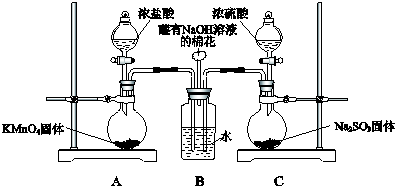
�ڿɼ�������1mol/L�����ܽ���ٽ����������嵼�뵽����ʯ��ˮ�У�������ʯ��ˮδ�����ǣ������1������������ʯ��ˮ����ǣ������2�����3������
����ٷ�Ӧ����Թܵ���1��2��Ʒ����Һ������Ʒ����ɫ�������3��������Ʒ�첻��ɫ�������2������
�ʴ�Ϊ��
| ʵ�鲽�� | Ԥ������ͽ��� | |
| �� | ��������1mol/L�����ܽ���ٽ����������嵼�뵽����ʯ��ˮ�� | ��1��������ʯ��ˮδ�����ǣ������1������ ��2��������ʯ��ˮ����ǣ������2�����3���� |
| �� | ����ٷ�Ӧ����Թܵ���1��2��Ʒ����Һ���� | ��1����Ʒ����ɫ�������3������ ��2����Ʒ�첻��ɫ�������2���� |
���� ���⿼�������Ʊ���������ԭ��Ӧ���������̽��ʵ�飬�ؼ�����ȷʵ��ԭ����������ѧ����ʵ�������Ŀ��飬�Ѷ��еȣ�ע���������ʵ����ʣ�


 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��v��H2��=v��H2O��ʱ���ﵽƽ�� | |
| B�� | �����¶ȣ�����Ӧ���ʼ�С���淴Ӧ��������ѧƽ�������ƶ� | |
| C�� | ʹ�ø�Ч���������NO��ƽ��ת���� | |
| D�� | ��ѧƽ�ⳣ������ʽΪK=$\frac{c��{N}_{2}��•{c}^{4}��{H}_{2}O��}{c��S{O}_{2}��•{c}^{2}��NO��•{c}^{4}��{H}_{2}��}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
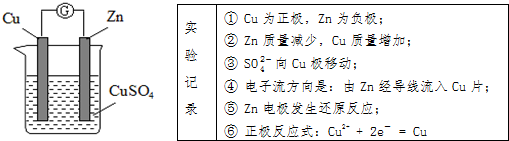
| A�� | �ڢۢ� | B�� | �٢ڢܢ� | C�� | �٢ڢܢ� | D�� | �ڢۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
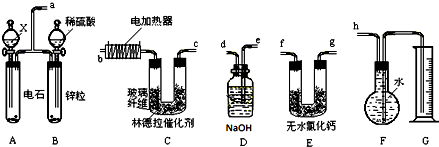
| A�� | ʯ�͡�ú����Ȼ������֬�����ڻ�ʯȼ�� | |
| B�� | ��֬�ڼ��������µ�ˮ�ⷴӦ�ֳ�Ϊ������Ӧ | |
| C�� | ����ʽΪ��C6H10O5��n�ĵ��ۺ���ά�ػ�Ϊͬ���칹 | |
| D�� | �����ǻ�ԭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
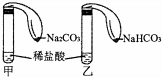 Ϊ�Ա�Na2CO3��NaHCO3�����ʣ�ʵ��С���ͬѧ���ڼס�����֧�Թ��зֱ��������ϡ���ᣬ�������ֱ�װ��Na2CO3��NaHCO3��ĩ��С����ֱ�������֧�Թܿڣ��������ڵ�Na2CO3��NaHCO3�����Թ��У���ͼ����
Ϊ�Ա�Na2CO3��NaHCO3�����ʣ�ʵ��С���ͬѧ���ڼס�����֧�Թ��зֱ��������ϡ���ᣬ�������ֱ�װ��Na2CO3��NaHCO3��ĩ��С����ֱ�������֧�Թܿڣ��������ڵ�Na2CO3��NaHCO3�����Թ��У���ͼ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͬ������NaHCO3��Na2CO3�� �ȶ� | |
| B�� | �������Na2CO3��NaHCO3�����зֱ�μ�ͬŨ�ȵ����ᣬ���߲����������ʿ� | |
| C�� | ��ͬ������NaHCO3��Na2CO3��������ˮ | |
| D�� | ��ʵ��ⶨ��Na2CO3��Һ�Լ��ԣ�˵��Na2CO3���ڼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4��mol/L�� 2 | B�� | 16��mol/L�� 2 | C�� | 20��mol/L�� 2 | D�� | 25��mol/L�� 2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com