
| 滴定次数 | 0.050 00 mol·L-1 Na2S2O3标准溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | |
| 1 | 0.00 | 20.04 |
| 2 | 0.12 | 20.08 |
| 3 | 0.05 | 20.05 |
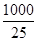 =0.040 mol.
=0.040 mol.

科目:高中化学 来源:不详 题型:单选题
| A.汽油失火时,立即用水灭火 |
| B.电线短路失火时,要用泡沫灭火器灭火 |
| C.浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
| D.浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用反应物、产物中键能数据可判断对应反应的反应热 |
| B.用沸点数据推测将一些液体混合物用分镏的方法分离开来的可能性 |
| C.用反应热数据的大小判断不同反应的反应速率的快慢 |
| D.用平衡时各组分的物质的量浓度可计算一定温度下反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.烧碱---爆炸品 | B.浓硫酸---剧毒品 | C.汽油---腐蚀品 | D.酒精---易燃品 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
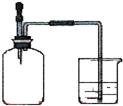
| A.①②③④⑤ | B.①②④ | C.①③④⑤ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
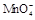 在酸性环境下的还原产物是
在酸性环境下的还原产物是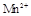 ;②草酸是二元弱酸。
;②草酸是二元弱酸。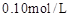 的草酸溶液
的草酸溶液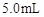 ,按下表中四种方案分别加入相应的试剂,使其发生反应。四支试管中均可观察到有气泡产生,且溶液的颜色变化都为:紫红色→红色→橙红色→橙色→黄色→无色,溶液褪为无色所需的时间如下表所示(表中“—”表示未加入该试剂)。
,按下表中四种方案分别加入相应的试剂,使其发生反应。四支试管中均可观察到有气泡产生,且溶液的颜色变化都为:紫红色→红色→橙红色→橙色→黄色→无色,溶液褪为无色所需的时间如下表所示(表中“—”表示未加入该试剂)。| 实验 编号 | 反应温度 (利用水浴加热) | 稀硫酸溶液 |  固体 固体 | 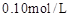 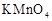 溶液 溶液 | 褪色时间 |
| 1 | 65℃ | — | — | 1.0mL | 100s |
| 2 | 65℃ | 10滴 | — | 1.0mL | 90s |
| 3 | 75℃ | 10滴 | — | 1.0mL | 40s |
| 4 | 75℃ | 10滴 | 加入少许 | 1.0mL | 3s |
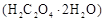 样品
样品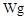 ;配制成
;配制成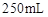 溶液;每次移取25.00mL该溶液于锥形瓶中,用0.10mol/L酸性高锰酸钾溶液滴定;滴定实验重复操作2—3次。请回答:
溶液;每次移取25.00mL该溶液于锥形瓶中,用0.10mol/L酸性高锰酸钾溶液滴定;滴定实验重复操作2—3次。请回答: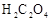 溶液与酸性
溶液与酸性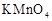 溶液反应的离子方程式为_________。
溶液反应的离子方程式为_________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.未冷却即转移、定容 | B.未洗涤烧杯和玻璃棒 |
| C.定容时仰视刻度线观察液面 | D.容量瓶中原来含有少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.①②③④ | C.①③④ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.减压过滤是为了加快过滤速率,得到较大颗粒的晶体 |
| B.硫酸亚铁铵晶体过滤后用无水乙醇洗涤 |
| C.纸层析法分离铁离子和铜离子实验中,展开剂的成份为蒸馏水与丙酮 |
| D.欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得硝酸钾晶体;将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com