
 ;
; .
. 分析 由于单体经过某些化学反应(如加聚、缩聚、开环等)生成高聚物,所以在高分子链中,单体转变为在化学组成上能够重复的最小单位,即链节.判断高聚物的单体,就是根据高分子链,结合单体间可能发生的反应机理,找出高分子链中的链节,判断其单体.
①凡链节主链只有两个碳原子(无其他原子)的聚合物,其合成单体必为一种,将两个半键闭合即可.
②凡链节主链有四个碳原子(无其他原子),且链节无双键的聚合物,其单体必为两种,在中央画线断开,然后两键闭合即可.
③凡链节主链上只有碳原子,仅存在碳碳双键结构的高聚物,其规律是“凡双键,四个碳;无双键,两个碳”画线断开.
解答 解:(1) 的单体是:CH2=CH2;
的单体是:CH2=CH2; ;
;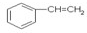 ,故答案为:CH2=CH2;
,故答案为:CH2=CH2; ;
; ;
;
(2) 的单体是CH2=CH2;
的单体是CH2=CH2; ,故答案为:CH2=CH2;
,故答案为:CH2=CH2; .
.
点评 本题考查根据聚合反应产物判断其单体的方法,题目难度中等,解题根据是明确高分子化合物为加聚反应还是缩聚反应产物,然后根据反应特点找出单体即可.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl-,AlO2-,SO32-,Na+ | B. | NO3-,CH3COO-,Na+,NH4+ | ||
| C. | Cl-,NO3-,Mg2+,K+ | D. | SO42-,HCO3-,Cl-,K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl,④NH3•H2O,c(NH4+)由大到小的顺序是:①>③>②>④ | |
| B. | 常温时,将等体积的盐酸和氨水混合后pH=7,则c (NH4+)>c (Cl-) | |
| C. | 0.2 mol•L-1Na2CO3溶液中:c (CO32-)+c (HCO3-)+c (H2CO3)=0.2 mol•L-1 | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到酸性溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用图甲所示装置制取并收集少量的N02气体(不考虑倒吸) | |
| B. | 用图乙所示装置制取并收集氨气 | |
| C. | 用图丙所示装置用苯萃取碘水中的碘,并将碘的苯溶液从漏斗下口放出 | |
| D. | 用图丁所示装置配制一定物质的量浓度的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:填空题
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的PH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2,△H= kJ·mol-1。

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g)△H=Q1 kJ/mol | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2 kJ/mol | K2 | 2.38 | 1.72 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g)△H=QkJ/mol | K | ? | ? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com