
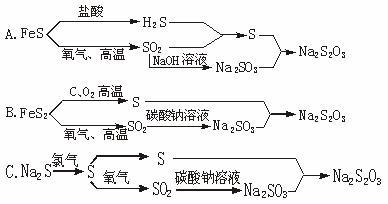
(1)请你从中选择最为合理的生产流程,并简要说明理由。
(2)若由原料S的转化率为75%,制SO2的转化率为90%,SO2制Na2SO3的转化率为95%,则用于制S和Na2SO3的原料质量比为多少,才能最多地制得Na2S2O3?(其他消耗不计)
解析:(1)欲判断提供的流程中的哪一种更适合于化工生产,则应从原料来源的难易、价格的高低、工艺的复杂性等综合考虑。流程A中的FeS在自然界中没有现存矿产,来源受阻。用H2S和SO2制备S不适合工业化生产。NaOH的价格远比Na2CO3的高,用NaOH吸收SO2制Na2SO3会加大生产成本。
流程B的原料是黄铁矿,这是一种自然矿料,来源广,价格低,适用于S和SO2的生产,且用碳酸钠替代NaOH吸收SO2,降低了生产成本。
流程C中的原料是Na2S,自然界中没有,是一种二级工业原料,价高量少,不利于大规模生产,更何况用氯气制S也不适合工业生产要求。根据以上分析,流程B具有原料来源丰富、价格低、工艺简单成熟的优点,是三种流程中较优的一种。
(2)设1 mol FeS2原料中有x用于制S,则有1 mol-x的FeS2用于制备Na2SO3。根据FeS2~2S及FeS2~2SO2~2Na2SO3可得生成S的物质的量n(S)=2x×0.75=1.5x,生成Na2SO3的物质的量n(Na2SO3)=2×(1 mol-x)×0.9×0.95=1.71 mol-1.71x,由反应Na2SO3+S====Na2S2O3知,若要最多地制得Na2S2O3,必须满足n(S)=n(Na2SO3),即1.5x=1.71 mol-1.71x,解之得x=0.533 mol。因同种物质的物质的量之比等于其质量比,故用于制S和Na2SO3的原料质量比为1.14∶1。
答案:(1)B(理由见解析) (2)1.14∶1


 全能测控一本好卷系列答案
全能测控一本好卷系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com