
| A. | 碳氢化合物的通式为CnH2n+2 | |
| B. | 燃烧产物为CO2和H2O的化合物一定是碳氢化合物 | |
| C. | 碳原子间以单键相连的烃是烷烃 | |
| D. | 烷烃分子的相对分子质量一定是偶数 |
分析 A、碳氢化合物包括烷烃、烯烃和炔烃;
B、燃烧产物为CO2和H2O的化合物不仅有碳氢化合物,还有烃的衍生物;
C、并不是所有碳氢化合物中都存在碳碳单键;
D、烷烃的分子组成通式符合CnH2n+2,烷烃分子的相对分子质量为14n+2.
解答 解:A、只有烷烃的分子组成通式符合CnH2n+2,烯烃分子组成通式为CnH2n,炔烃分子组成通式为CnH2n-2,故A错误;
B、燃烧产物为CO2和H2O的化合物不仅有碳氢化合物,还有烃的衍生物,例如:糖类、酯等物质,故B错误;
C、并不是所有碳氢化合物中都存在碳碳单键,如甲烷分子中只含有一个碳原子,不存在碳碳键,故C错误;
D、烷烃的分子组成通式符合CnH2n+2,烷烃分子的相对分子质量为14n+2,一定是偶数,故D正确.
故选D.
点评 本题考查学生碳氢化合物的类别以及通式、成键情况等方面的知识,属于综合知识的考查,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4的摩尔质量为16g | |
| B. | 标准状况下,18 g H2O的体积是22.4 L | |
| C. | 17 g NH3的物质的量是1 mol | |
| D. | 阿伏加德罗常数约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
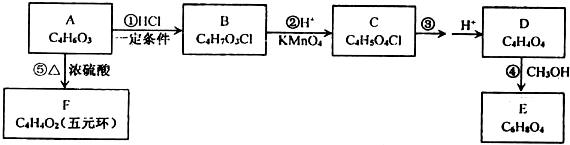
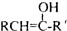 (R和 R′,代表烷基或 H)不稳定,本题各物质均不考虑此类结构.
(R和 R′,代表烷基或 H)不稳定,本题各物质均不考虑此类结构. 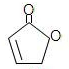 E(反式):
E(反式):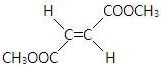
 .
.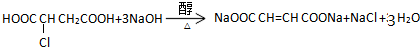 .
. .
.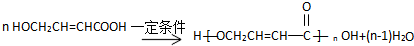 .
.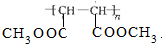 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
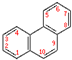 .它的一氯代物有5种.
.它的一氯代物有5种.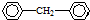 ,试再写出另一种的结构简式
,试再写出另一种的结构简式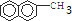 .
.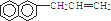 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
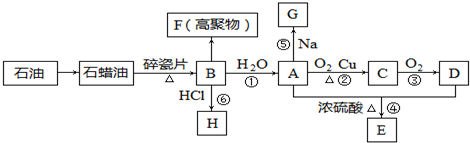
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡比氢氧化钙的碱性强 | |
| B. | HBrO4的酸性比HIO4强 | |
| C. | 铍(Be)原子失电子的能力比镁弱 | |
| D. | 硒(Se)化氢的稳定性比硫化氢的稳定性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
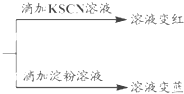
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO和HCl | B. | NH4Cl和HCl | C. | NH4Cl和HClO | D. | NH4Cl和HClO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com