
| A.原子半径:Na<Mg<Al<F |
| B.酸性强弱:H2SiO3<H2CO3<H3PO4<H2SO4 |
| C.热稳定性:HCl>H2S>PH3>AsH3 |
| D.碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.在卤化氢中HF最稳定 |
| B.一个D2O分子所含的中子数为8 |
| C.稳定性:H2S>HF |
D.HCl的电子式为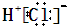 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.D在过量的B中燃烧的主要产物为DB? | ||||
| B.C的氢化物的水溶液酸性比E的强 | ||||
C.A与B形成的阴离子可能有A
| ||||
| D.E单质中由于形成了氢键,所以很容易液化 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.原子半径:e<N<OB. |
| B.非金属性si<P<S |
| C.还原性:SiH4<PH3<HClD. |
| D.酸性:H4SiO4<H3PO4<H2SO4. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素周期表有十八个纵行,所以有十八个族 |
| B.短周期元素指第四、五、六周期的元素 |
| C.第ⅠA族的元素全部是金属元素 |
| D.元素性质的周期性变化是元素原子核外电子排布周期性变化的必然结果 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲与水反应比乙与水反应剧烈 |
| B.甲单质能从乙的盐溶液中置换出单质乙 |
| C.与某非金属反应时甲原子失电子数目比乙的多 |
| D.甲的最高价氧化物的水化物比乙的最高价氧化物的水化物碱性强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com