

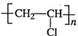 ,CH2C=HC-CN.
,CH2C=HC-CN.分析 根据题中各物质转化关系,A和HCN发生加成反应生成C,A与F生成D,C和D反应生成人造羊毛,故D是CH2=CH-OOCCH3,C是H2C=HC-CN,逆推可得A是乙炔、E是CH3COOH.乙炔与氯化氢发生加成反应生成B为氯乙烯,氯乙烯发生加聚反应生成聚氯乙烯PVC为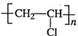 ,据此解答
,据此解答
解答 解:根据题中各物质转化关系,A和HCN发生加成反应生成C,A与F生成D,C和D反应生成人造羊毛,故D是CH2=CH-OOCCH3,C是H2C=HC-CN,逆推可得A是乙炔、E是CH3COOH.乙炔与氯化氢发生加成反应生成B为氯乙烯,氯乙烯发生加聚反应生成聚氯乙烯PVC为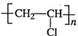 ,
,
(1)反应①是乙炔与氯化氢放出加成反应生成B为氯乙烯,反应②是CH2=CH-OOCCH3与H2C=HC-CN发生加聚反应生成高聚物人造羊毛,
故答案为:加成反应;加聚反应;
(2)由上述分析可知,PVC为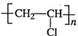 ,C为H2C=HC-CN,
,C为H2C=HC-CN,
故答案为: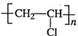 ;H2C=HC-CN;
;H2C=HC-CN;
(3)A→D是乙炔与CH3COOH发生加成反应生成CH2=CH-OOCCH3,反应的化学反应方程式为:HC≡CH+CH3COOH$\stackrel{催化剂}{→}$H2C=CH-OOCCH3,
故答案为:HC≡CH+CH3COOH$\stackrel{催化剂}{→}$H2C=CH-OOCCH3;
(4)D是CH2=CH-OOCCH3,与D互为同分异构体且可发生碱性水解的物质,该物质含有酯基(不包括环状化合物),可能结构有:CH2=CHCOOCH3、CH2=CHCH2OOCH、CH3CH=CHOOCH、CH2=C(CH3)OOCH,
故答案为:4;CH2=CHCOOCH3 或CH2=CHCH2OOCH或CH3CH=CHOOCH或CH2=C(CH3)OOCH.
点评 本题考查有机物的推断,涉及炔、烯等物质的性质、同分异构体的书写、高聚物等,难度中等,根据人造羊毛的结构确定C、D的结构简式是解题关键,注意采用倒推和正推向结合的方法推断.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g过氧化钠含有的共用电子对数为0.2NA | |
| B. | 2H2O2(l)=2H2O(l)+O2(g)△H=-98.2 kJ •mol-1,△S=70.5 J•mol-1•K-1,该反应低温能自发进行 | |
| C. | 过氧化氢使高锰酸钾溶液褪色,1mol过氧化氢得到2NA电子 | |
| D. | 在含有NH4+、Ba2+、Cl-、NO3-离子的溶液 加入少量过氧化钠以上各离子量几乎不减 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广利用太阳能、风能的城市照明系统,发展低碳经济和循环经济,有利于改善环境质量 | |
| B. | 油脂在碱的作用下可发生水解,工业上利用该反应生产肥皂 | |
| C. | 处理废水时可加入明矾作为混凝剂,以吸附水中的杂质 | |
| D. | 硬铝、碳素钢都是合金材料;合成纤维、光导纤维都是有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉和纤维素互为同分异构体 | |
| B. | 糖类、油脂和蛋白质是基本营养物质,它们都是天然高分子化合物 | |
| C. | 可以用溴水鉴别苯、CCl4和无水乙醇 | |
| D. | 苯可以发生取代反应和加成反应,但是无法发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 酸 | 醋酸 | 次氯酸 | 亚硝酸 |
| 电离常数(Ka) | 1.7×10-5 | 3.0×10-8 | 7.1×10-4 |
| A. | PH相同的氯水和亚硝酸溶液,水电离出的c(H+)相同 | |
| B. | 往氯水滴加NaOH溶液呈中性:c(Na+)=2(ClO-)+c(HClO) | |
| C. | 浓度相等的CH3COONa和NaNO2两份溶液中;c(CH3COO)->c(NO${\;}_{2}^{-}$) | |
| D. | 向pH=a的醋酸溶液中加一定量水,所得溶液的pH>a、pH<a、pH=a均有可能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol/L Na2CO3溶液中,阴离子总数大于0.1 NA | |
| B. | 常温常压下,1 mol甘氨酸中含C-H键数目为3 NA | |
| C. | 标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1 NA | |
| D. | 50℃时,10 L pH=13的NaOH溶液中含有的OH-数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质或离子 | 能否共存 | 原因解释 |
| A | 常温常压下:NH3、O3、H2、HCl | 不能共存 | NH3为碱性气体,HCl为酸性气体,发生的反应为:NH3+HCl=NH4Cl |
| B | 水溶液中:K+、Ag+、NO3-、NH3•H2O | 不能共存 | 发生反应的离子方程式为:Ag++OH-=AgOH↓ |
| C | 水电离出的c(OH-)=1×10-13mol/L的溶液中:Fe2+、MnO4-、SO42-、Na+ | 不能共存 | 只可能发生反应:Fe2++2OH-=Fe(OH)2↓ |
| D | 溶液中:Al3+、Na+、SO42-、CO32- | 可以共存 | 不能发生反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 尿素是蛋白质代谢的产物,也是重要的化学肥料,工业合成尿素反应如下:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)
尿素是蛋白质代谢的产物,也是重要的化学肥料,工业合成尿素反应如下:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度(10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com