
关于下图的说法正确的是

A.构成原电池时Cu是负极
B.构成电解池时Cu是阴极
C.构成电解池时质量增重的极是阴极
D.电池工作时溶液中的 一定移向Cu极
一定移向Cu极
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014江苏省南京市雨花区高一下学期期末考试化学试卷(解析版) 题型:选择题
下列物质中能与溴水发生化学反应而使褪色的是
A.苯 B.四氯化碳 C.乙烯 D.乙醇
查看答案和解析>>
科目:高中化学 来源:2013-2014广西贵港市毕业班5月高考冲刺模拟理综化学试卷(解析版) 题型:选择题
下列实验操作不能达到预期的目的的是
| 实验目的 | 操作 |
A | 证明CH2=CHCH2OH中含有碳碳双键 | 滴入溴水 |
B | 欲证明浓硫酸有脱水性和强氧化性 | 将浓硫酸滴到蔗糖上 |
C | 证明FeCl2溶液中含有Fe2+ | 加入酸性KMnO4溶液 |
D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
查看答案和解析>>
科目:高中化学 来源:2013-2014广西桂林市下学期高二年级期末考试化学试卷(解析版) 题型:选择题
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据电镀原理,钢芯镀镍时,钢芯应该做
A.正极 B.负极 C.阳极 D.阴极
查看答案和解析>>
科目:高中化学 来源:2013-2014广西桂林市、崇左市、防城港市、北海市高三化学试卷(解析版) 题型:推断题
(15分)芳香烃M的相对分子质量为92,是一种重要的有机黄原料,某工厂以它为初始原料设计出如下合成路线图(部分产物,反应条件省略)。其中A是一氯代物。

已知:Ⅰ
Ⅱ (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与题中所给信息回答下列问题:
(1)M的结构简式是 ;M→A的反应条件是 。
(2)A中的共面原子最多 个。
(3)写出反应④的化学山程式 。
(4)②的反应类型属于 ;②和③的反应顺序 (填“能”或“不能”)颠倒。
(5)  有多种同分异构体,写出2种含有1个醛基和2个羟基,苯环上只能生成2种一氯取代物的芳香族化合物的结构简式: 。
有多种同分异构体,写出2种含有1个醛基和2个羟基,苯环上只能生成2种一氯取代物的芳香族化合物的结构简式: 。
(6)写出由A转化为 的合成路线(用
的合成路线(用 表示,并在箭号上写明反应试剂及反应条件)。
表示,并在箭号上写明反应试剂及反应条件)。
查看答案和解析>>
科目:高中化学 来源:2013-2014广西桂林市、崇左市、防城港市、北海市高三化学试卷(解析版) 题型:选择题
在673K、30MPa下,在密闭容器中进行合成氨反应: N2(g)+3H2(g) 2NH3(g) △H<0,n(NH3)和n(H2)随时间(t)的变化关系如右图所示。下列分析一定正确的是
2NH3(g) △H<0,n(NH3)和n(H2)随时间(t)的变化关系如右图所示。下列分析一定正确的是
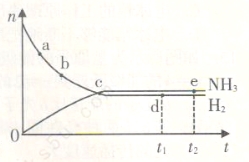
A、正反应速率:a点小于b点
B、c点处反应达到平衡
C、d点和e点处的n(N2)不一样
D、若其他条件不变,在773 K时反应至t1时刻,n(H2)比图中d点对应的n(H2)大
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷(解析版) 题型:实验题
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
接 , 接 , 接 ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?
乙中 ____ ,丙中 ______ ;
(3)丁中酸性KMnO4溶液的作用是 ;
(4)写出甲中反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
14分)某实验小组用0.50 mol·L- 1 NaOH溶液和0.50mol·L- 1 的硫酸溶液进行中和热的测定。 Ⅰ.配制0.50mol·L- 1 硫酸溶液
Ⅰ.配制0.50mol·L- 1 硫酸溶液
(1)若配制250 mL硫酸溶液,则须用量筒量取密度为1.84 g·cm- 3、质量分数为98%的浓硫酸 mL。
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如右图所示:
(2)仪器A的名称为 ;
(3)装置中碎泡沫塑料的作用是 ;
(4)写出该反应中和热的热化学方程式:(中和热为57.3 kJ·mol- 1) ;
(5)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①下表中的温度差平均值为 ℃;
②近似认为0.50mol·L- 1 NaOH溶液和0.50mol·L- 1 硫酸溶液的密度都是1g·cm- 3 ,中和后生成溶液的比热容c=" 4.18" J·(g·℃)- 1 。则中和热△H= (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol- 1 有偏差,产生此实验偏差的原因可能是(填字母) 。
| A.实验装置保温、隔热效果差 |
| B.量取NaOH溶液的体积时仰视读数 |
| C.一次性把NaOH溶液倒入盛有硫酸的小烧杯中 |
| D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com