
【题目】下列物质:①H3O+②[Cu(NH3)4]2+③CH3COO﹣④NH3⑤CO中存在配位键的是( )
A.①②
B.①②③
C.③④⑤
D.①②⑤
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是( )
A. 蒸馏操作时,冷凝水的方向应当由下往上
B. 分液操作时,首先要打开分液漏斗的上口活塞,或使活塞上的凹槽与上口部的小孔对准,然后进行分液
C. 过滤时,漏斗下端紧贴烧杯内壁
D. 提取碘水中的碘单质时,应选择有机萃取剂如乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH﹣的浓度变化曲线如图,下列说法正确的是( ) 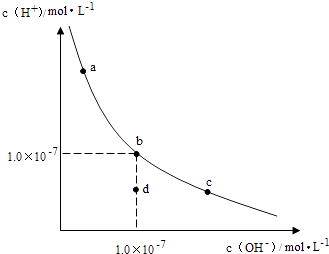
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10﹣13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1molL﹣1的NaOH溶液中,由水电离出的c(H+)=molL﹣1 , KW(25℃)KW(100℃)(填“>”、“<”或“=”).25℃时,向水的电离平衡体系中加入少量NH4HCO3固体,对水的电离平衡的影响是(填“促进”、“抑制”或“不影响”). 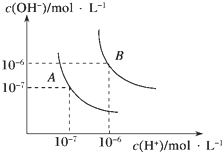
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置制取、提纯并收集下表中的四种气体(a、b、c、d表示相应仪器中加入的试剂,收集装置略去).其中可行的是( )
气体 | a | b | c | d | |
A | CO2 | 稀硫酸 | 石灰石 | 饱和Na2CO3溶液 | 浓H2SO4 |
B | Cl2 | 浓盐酸 | KMnO4固体 | 饱和NaCl溶液 | 浓H2SO4 |
C | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 碱石灰 |
D | H2 | 硝酸 | 锌粒 | H2O | P2O5 |
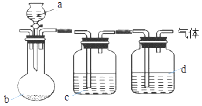
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其反应方程式为: HCOOH ![]() CO↑+H2O.
CO↑+H2O.
如图是制备一氧化碳还原三氧化二铁并检验反应产物结束时的实验装置.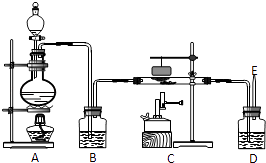
(1)实验前先检查装置的气密性;起始时应检验 , 以防止爆炸;
(2)装置B中盛放 , 除去;
(3)装置D中盛放 , 检验;
(4)写出C装置中反应的化学方程式;
(5)实验结束时应先停止处加热;
(6)在反应后磁铁悬挂在玻璃管上方,其作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图的实验装置可用于实验室中制取乙炔.请回答下列问题:
(1)图中,A管的作用是 , 制取乙炔的化学方程式为 .
(2)将制得的乙炔通入酸性KMnO4溶液中可观察到的现象是 , 这是由于乙炔发生了 反应.
(3)将制得的乙炔通入溴的四氯化碳溶液中可观察到的现象是 , 这是由于乙炔发生了 反应,写出该反应的化学方程式 .
(4) 为了安全,乙炔气体在点燃前应 , 乙炔燃烧时的现象是 . 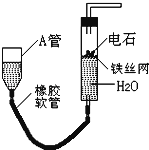
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25.00ml碱式滴定管中盛有溶液,液面恰好在20.00ml刻度处,现将滴定管中全部溶液放出,流入量筒内,所得溶液体积为( )
A.5mL
B.20 mL
C.大于5mL
D.小于5mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com