
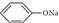
 ⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是( )
⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是( )| A. | ③①④②⑥⑤ | B. | ①③⑥④②⑤ | C. | ③②①⑥④⑤ | D. | ⑤⑥②④①③ |
科目:高中化学 来源: 题型:选择题
| A. | C2H2 | B. | C3H4 | C. | C4H6 | D. | C5H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | |||||||||||||||||
| D | E | I | |||||||||||||||
| B | C | F | H | G | |||||||||||||
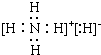 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ds原子在周期表中位于第7周期第Ⅷ族 | |
| B. | Ds是IB元素 | |
| C. | Ds元素为放射性元素 | |
| D. | Ds元素在元素周期表中d区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | Ba(NO3)2 溶于水,可将含有Ba(NO3)2 的废液倒入水槽中,再用水冲入下水道 | |
| C. | 用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| D. | 用滴管滴加液体时,滴管应垂悬在容器上方,不能触及容器内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两溶液稀释10倍后,pH相等 | |
| B. | 两溶液加热至相同的温度后,pH相等 | |
| C. | 两溶液中各加入等体积的pH等于5的HCl溶液后,pH相等 | |
| D. | 两溶液中水的离子积相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用Cu+2FeCl3=CuCl2+2FeCl2反应,设计一个原电池.
利用Cu+2FeCl3=CuCl2+2FeCl2反应,设计一个原电池.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com