
̼�������仯�����ڹ�ũҵ����������������Ҫ���á���ش��������⣺
��1����CH4 ����ԭNOx �������������������Ⱦ�����磺
CH4(g) + 4NO2(g) = 4NO(g)��CO2(g) + 2H2O(g) ��H1����574 kJ��mol��1
CH4(g) + 4NO(g) = 2 N2(g)��CO2(g) + 2H2O(g) ��H2
��2 mol CH4 ��ԭNO2 ��N2�����������зų�������Ϊ1734 kJ����H2�� ��
��2���ݱ�������ѧ����һ������������Fe2O3����鷴Ӧ����ȡ���������Ľ��������䷴Ӧ���£� Fe2O3(s) + 3CH4(g)  2Fe(s) + 3CO(g) +6H2(g) ��H>0
2Fe(s) + 3CO(g) +6H2(g) ��H>0
�� ����Ӧ��5L���ܱ������н��У�1min��ﵽƽ�⣬���Fe2O3�ڷ�Ӧ����������3.2g����ö�ʱ����CO��ƽ����Ӧ����Ϊ ________________ ��
�� ���÷�Ӧ�ں��º�ѹ�����н��У��ܱ����÷�Ӧ�ﵽƽ��״̬����_____(ѡ�����)
a��CH4��ת���ʵ���CO�IJ���
b����������ƽ����Է�����������
c��v��CO����v��H2���ı�ֵ����
d�����������������
�� �÷�Ӧ�ﵽƽ��ʱij���������¶ȱ仯��ͼ��ʾ�����¶���T1���ߵ�T2ʱ��ƽ�ⳣ��KA ______KB���>������ <����=��������������Ա�ʾ������������Щ ��
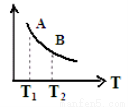
a��H2���淴Ӧ����
b��CH4�ĵ��������
c����������ƽ����Է�������
��3������20mL 0.0lmol��L-l������HNO2��Һ����μ���һ��Ũ�ȵ��ռ���Һ����û����Һ���¶ȱ仯��ͼ��ʾ�������й�˵����ȷ����________
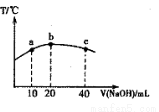
�ٸ��ռ���Һ��Ũ��Ϊ0.02mol��L-1
�ڸ��ռ���Һ��Ũ��Ϊ0.01mol��L-1
�� HNO2�ĵ���ƽ�ⳣ����b��>a��
�ܴ�b�㵽c�㣬�����Һ��һֱ���ڣ�c(Na+)>c(NO2-)>c(OH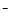 )> c(H+)
)> c(H+)

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�����и߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
һֻ���Ϊa mL�ĵζ��ܣ�����첿�ֳ�����Һ������Һ����m mL������Һ�潵��n mL��ʱ�������ж���ȷ����
A��������Һ�����Ϊ(m��n) mL B��������Һ�����Ϊ(n��m) mL
C��������Һ�������(a��n) mL D��������Һ�������n mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����Ȫʮ���и�����һ�νο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�±��У��Գ��������ȷ�Լ����������ϵ���жϣ���ȫ��ȷ����
ѡ�� | ������ | ������ | �ж� |
A | ���ƴ�����ò�Ҫʢ�����Ի���Խ�ǿ��Һ��ʳ�� | ��ΪAl��Al2O3�ȿ������ᷴӦ���ֿ�����Ӧ | ��ԣ���ԣ��� |
B | �����ھƾ��ƻ����ϼ����ۻ��������� | �������ۻ������н�ǿ���������� | ��ԣ���ԣ��� |
C | ��ХʹˮԴ������Ⱦ�����������������;��� | ��Ϊ����ˮ������Al(OH)3���壬���������� | ��ԣ�������� |
D | �������ƳɵIJ۳������ܷ�����Ũ�����Ũ���� | ��Ϊ������������Ũ�����Ũ���ᷴӦ | �������ԣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ�����У���ȷ����
A����ϩ�Ľṹ��ʽ��C2H4 B������Ľṹʽ��CH3CH3
C���ǻ���OH�� D������ķ���ʽ��C2H4O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��CH3COOH(l)��2O2(g)===2CO2(g)��2H2O(l�� ��H1����870��3 kJ/mol
��C(s)��O2(g)===CO2(g�� ��H2����393��5 kJ/mol
��H2(g)�� O2(g)===H2O(l�� ��H3����285��8 kJ/mol
O2(g)===H2O(l�� ��H3����285��8 kJ/mol
��2C(s)��2H2(g)��O2(g)===CH3COOH(l)�ķ�Ӧ��Ϊ
A����870��3 kJ/mol B����571��6 kJ/mol
C��+787��0 kJ/mol D����488��3 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����һ�и������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A����ˮ��Һ���ܵ����H+�Ļ�����һ��������
B��CaCl2��NaOH��HCl��HD�������ʶ����ڻ�����
C��Na2O2��Na2O�����ڼ���������
D���з��⡢���ȡ���ɫ������������������ը������IJ�һ���ǻ�ѧ�仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��̫ԭ���и߶��ϵ�һ�ܿ����ƻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������仯ʾ��ͼ������ѡ����ȷ����
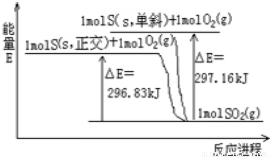
A��S��s����б��+O2��g��=SO2��g����H=+297��16 kJ•mol-1
B��S��s����б��+O2��g��=SO2��g����H=-296��83 kJ•mol-1
C��S��s��������+O2��g��=SO2��g����H=-296��83 kJ•mol-1
D����б�����������ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��һ��ѧ����ѧ�Ծ��������棩 ���ͣ�������
0��40LijŨ�ȵ�NaOH��Һǡ�����״����5��8 L Cl2��ȫ��Ӧ�����㣺
��1�����ɵ�NaClO�����ʵ�����
��2������Һ��NaOH�����ʵ���Ũ�ȡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�������һ������ָ�������д����������
A����c(HCO3-)=0.1 mol��L-1����Һ�У�NH4+��AlO2-��Cl-��NO3-
B�������£�����ˮ�������c(H+)=1��10-12 mol��L-1����Һ�У�Fe2+��ClO-��Na+��SO42?
C���ڼ������۲���H2����Һ�У�SO42-��NO3-��Na+��NH4+
D����ʹ��ɫʯ����ֽ��������Һ�У�SO32-��CO32-��Na+��K+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com